【工作概述】
锂-硫电池因其超高的理论能量密度而备受瞩目。在锂-硫体系中,电解液不仅负责锂离子的传输,更会显著影响正负极的反应机理和工作状态,因此需要重新审视并设计锂-硫电池电解液,以实现锂-硫电池的长久稳定工作和高能量密度。基于此,北京大学庞全全课题组联合Doron Aurbach课题组总结了锂-硫电解液方面的最新研究成果,根据多硫化锂在电解液中的溶解度,将电解液分为微溶型电解液(Sparingly solvating electrolytes)、中溶型电解液(Moderately solvating electrolytes)和高溶型电解液(Highly solvating electrolytes),并从电解液结构、溶剂化能力、电解液用量、硫电极反应机理和对锂稳定性等角度对这三类电解液进行了详细的探讨和分析。该综述文章以“Electrolyte solutions design for lithium-sulfur batteries”为题发表在国际顶级能源期刊Joule上,第一作者为刘亚涛。
【内容表述】
在锂-硫电池中,锂负极和硫正极均为溶解-沉积式的反应机理,电解液会强烈地参与到正负两极的电化学反应中,并最终影响电池的循环寿命和能量密度。首先,负极的工作状态与电解液性能密切相关,包括锂的剥离/沉积行为、固态电解质界面膜(SEI)的生成、锂与溶剂的副反应等;其次,多硫化锂在电解液中的溶解度是决定其溶解/穿梭的根本原因,并影响硫电极的反应路径/机理;最后,电解液对多硫化锂的溶解能力是决定其用量(即液/硫比)的重要因素(图1 A)。
面对提高锂-硫电池能量密度的迫切需求,电解液用量必须得到有效降低。比如500 Wh/kg、700 Wh/L的软包锂硫电池对应的液/硫比约为1 μL/mg,然而目前报道的扣式和软包锂硫电池的液硫比远高于此值。以常规的低浓度醚类电解液为例(1 M LiTFSI, 0.2 M LiNO3溶于等体积比的乙二醇二甲醚和1,3-二氧戊环),Li2S8在该电解液中的溶解度约为6.6 M(以硫原子数计),此时对应的是液/硫比为4.7 μL/mg。液/硫比较高时,硫电极具有较好的反应动力学;液/硫比较低会导致多硫化锂的溶解达到饱和,出现电解液粘度增大、离子电导率降低、硫化锂沉积过电势增大等一系列问题。常规低浓度醚类电解液的复杂性和困难性即体现于此。
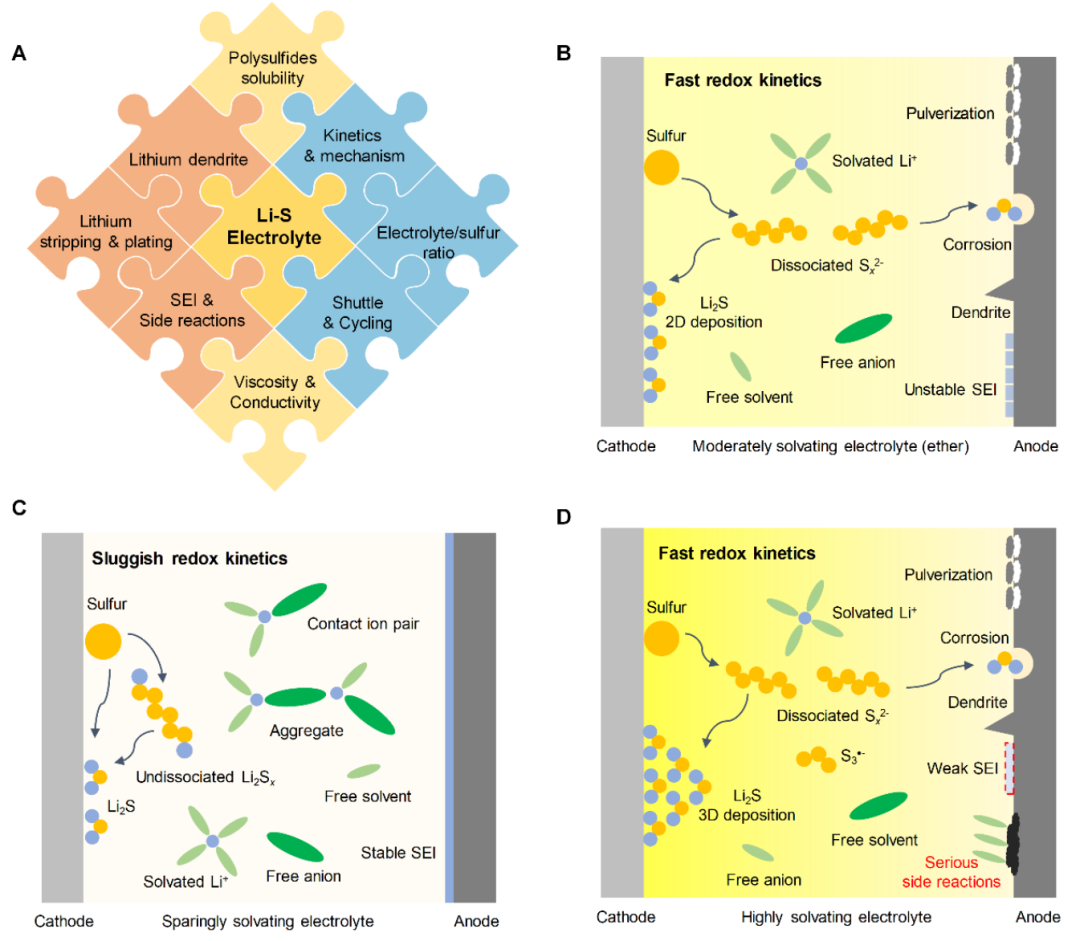
图1. 电解液在锂-硫电池中的作用。(A)以拼图的形式展示出电解液与锂负极、硫正极和电池性能环环相扣的紧密联系,(B)中溶型电解液,(C)微溶型电解液,(D)高溶型电解液
基于以上讨论,文章认为电解液对多硫化锂的溶解能力或者多硫化锂在电解液中的溶解度是考量和重新设计锂-硫电解液的重要标准,并以此为依据将目前公开报道的锂-硫电解液划分为微溶、中溶和高溶三种类型。
1 影响多硫化锂溶解的因素
在讨论三种类型的电解液之前,文章具体分析了影响多硫化锂溶解行为的因素。首先,溶剂的极性(以介电常数ε描述)或路易斯碱性(以给体数DN描述)是影响多硫化锂溶解的首要因素,比如二甲基亚砜(ε=46.5、DN=29.8)对多硫化锂的溶解能力(14.25 M Li2S8,以硫原子计)强于乙二醇二甲醚(ε=7.1、DN=20)。其次,电解质盐会影响多硫化锂的溶解行为,在低浓度体系中,某些盐可以与多硫化锂配位或者形成氢键(如NH4NO3),提高多硫化锂的溶解度;当电解质盐的浓度较高时,多硫化锂的溶解会被明显抑制,典型的如近饱和的二乙二醇二甲醚电解液。再次,不同链长的多硫化锂具有不同的溶解行为,链越短,硫和锂之间的作用力越强,溶解越难。此外,短链的多硫化锂易形成二聚体或者多聚体,阻碍锂与溶剂分子的相互作用,降低溶解度。
2 中溶型电解液(常规醚类)
中溶型电解液的典型代表为低浓度的醚类电解液体系。在该体系中,硫在充放电过程中表现为溶解-沉积式的反应机理,文章详细描述了硫/多硫化锂的反应路径和与之对应的电化学反应方程式,并讨论了四个值得继续深入研究的机理问题:(1)多硫化锂的歧化反应和不同链长硫化锂之间的化学反应;(2)硫化锂的沉积;(3)Li2S2是否存在;(4)自由基阴离子(S3·-)的存在与作用。随后,文章重点阐述了醚类电解液在低电解液用量时面临的巨大挑战,包括:(1)高粘度和低离子电导率;(2)更严重的多硫化锂穿梭;(3)锂负极的腐蚀和电解液的消耗;(4)电催化剂的局限性。
3 微溶型电解液
微溶型电解液是指对多硫化锂有一定溶解能力,但溶解度非常低的溶液体系。目前对微溶电解液尚没有明确的定义或者标准,根据已发表的文献,Li2S8在此类电解液中的溶解度约为1-100 mM。文章重点介绍了五类微溶型电解液,分别为室温离子液体、溶剂化离子液体、高浓度盐溶液、氟化醚和含特殊锂盐的电解液,并详细分析了每一种电解液的组成、溶剂化结构、对多硫化锂的溶解能力、硫正极的反应机理和锂负极的稳定性。
微溶型电解液的优势在于可以从根本上解决多硫化锂的溶解穿梭,提高硫的利用率,并减缓多硫化锂对锂负极的腐蚀。而且,当多硫化锂的浓度降到非常低时,硫电极会由溶解-沉积转变为准固-固反应的机理,从而摆脱电解液用量对硫电极反应路径的依赖,达到降低液/硫比的目标。但与此同时,微溶型电解液同样面临着粘度大、离子电导率低、硫电极反应动力学慢等问题。
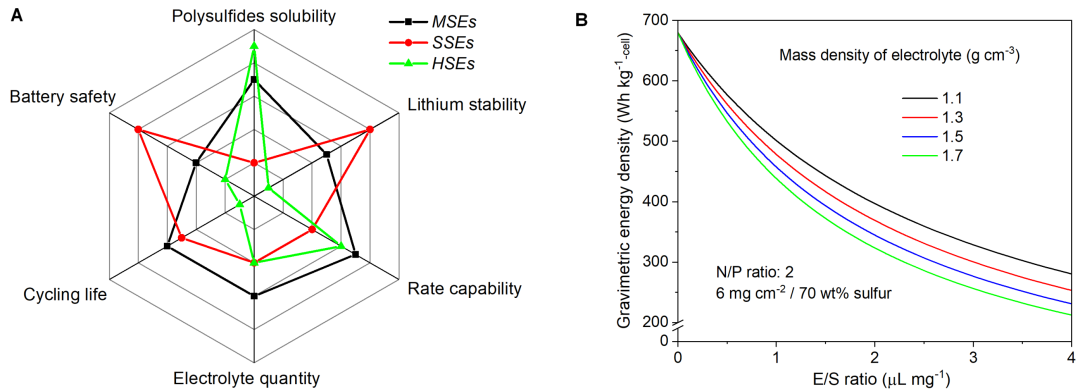
图2. (A)微溶、中溶和微溶型电解液的性能比较。(B)电解液密度对软包锂-硫电池能量密度的影响
4 高溶型电解液
高溶型电解液的构筑主要采用高介电常数或高给体数的溶剂,此外具有高给体数阴离子的锂盐也可以提高多硫化锂的溶解度。高溶型电解液的优势在于可以用较少的电解液溶解较多的多硫化锂,因此可以显著降低液/硫比。在高溶型电解液中,自由基阴离子(S3·-)在硫/多硫化锂的转化过程扮演者重要角色,而且在放电过程中硫化锂呈现为三维沉积,可以有效减缓硫电极表面的钝化。但是,高极性的溶剂与金属锂之间常常存在严重的副反应,因此锂负极的稳定性面临着更大的挑战。
【结论】
文章从多个角度综合比较了微溶、中溶和高溶型电解液在锂-硫电池中的表现,包括多硫化锂的溶解度、液/硫比、与锂负极的兼容性、电池的循环寿命、电池的倍率性能和电池的安全性能。简单来说,这三类电解液均具有明显的优势和劣势(图2 A),目前尚无法满足实用化的需求,这也反映出重新审视并设计锂-硫电池电解液的重要性和紧迫性。而且,文章指出目前主流的文章多用电解液体积来表征液/硫比,单位为mL/g,但是考虑到电解液密度的多样性(如常规低浓度醚类为1.1 g/cm3,近饱和的二乙二醇二甲醚为1.53 g/cm3),仅用体积无法准确评判不同电解液在整体电池中的质量占比(图2 B),因此建议采用电解液的质量(单位为g/g)对液/硫比进行描述。
文章最后对微溶、中溶和高溶三种电解液的发展给出了合理的建议,并再次强调电解液溶剂化能力对硫正极和锂负极的重要影响。在未来的研究中,利用机器学习大规模筛选溶剂和锂盐,通过原位的表征手段深入了解硫/多硫化锂的反应机理和路径,对于加快锂-硫电解液的发展至关重要。








暂无评论
发表评论