1 研究背景
目前市场上有超过130 种经食品和药物管理局 (FDA) 批准的蛋白质治疗剂,但细胞膜不透性在很大程度上限制了这些针对细胞外靶点的方法。细胞内蛋白质递送是生物医学应用和基础的变革性技术 研究。蛋白质在细胞信号转导和体内平衡中起关键作用,许多遗传性疾病是由异常的蛋白质功能引起的。
蛋白质递送的大多数细胞内靶点需要进入细胞质,包括递送至亚细胞器和细胞核。绝大多数细胞内递送策略依赖于修饰蛋白质或纳米载体的内体摄取。内体包埋严重限制了这些策略,隔离交付的货物并防止细胞质进入。包裹在内体中的货物通常会通过内/溶酶体途径被胞吐或降解,使内吞作用成为最终具有挑战性的摄取途径。最近的报告估计,只有不到 10% 的内吞货物会逃到胞质溶胶,这一结果可以通过设计用于触发内体破裂和逃逸的运载工具来改善。
递送载体与细胞膜的融合提供了一种直接的细胞内递送方式,绕过了与内体包埋相关的问题。脂质体载体可以与细胞膜融合,但面临与调理作用和加速血液清除相关的挑战。聚合物支架是多功能平台,可通过化学多样性提供设计灵活性。Francis 特别证明了通过将两亲聚合物与蛋白质进行位点选择性共轭来进行细胞内蛋白质递送。最近的其他方法利用阳离子树枝状大分子或含氟聚合物来协调和递送细胞质中的蛋白质,用于多种应用,包括癌症免疫治疗和治疗性基因编辑。
以前使用胍功能化的金纳米颗粒和用末端寡(谷氨酸)“E-tags”修饰的协同工程蛋白质实现了直接的胞质蛋白递送。在该系统中,静电胍-羧酸盐相互作用能够实现超分子复合物的自组装。该策略最近适用于胍基官能化聚(氧代降冰片烯)酰亚胺 (PONI) 聚合物(PONI-Guan,图 1),提供高效的细胞溶质递送,通过核共定位与成像流式细胞术和酶重组酶活性证明了几种 E 标记的蛋白质。然而,这两种策略都需要质粒工程来提供 E-tagged 蛋白质,从而产生与天然蛋白质完全不同的蛋白质,并使该策略变得繁琐。
四价生物素−链霉亲和素(STV)结合为蛋白质生物偶联提供了一种模块化的高亲和力策略。一个广泛的分子和大分子系统可以被生物素化,使其成为一个高度通用的生物偶联平台。我们在这里报道了使用生物素−链霉亲和素组装来提供蛋白质进入细胞的胞质传递。在该系统中,生物素化的寡核苷酸(谷氨酸)(bE20)和生物素化的蛋白首先与STV结合(图1)。
然后使用PONI-Guan均聚物将这些偶联物自组装,形成离散的(平均200−350nm)超分子聚合物−蛋白纳米复合材料。这些复合物通过生物素化的绿色荧光蛋白(b-GFP)的显微镜和核通路证明,促进了高效的胞质传递细胞。五种不同分子量、电荷和四级结构的额外荧光蛋白的细胞溶质传递证明了这种方法的多功能性。递送后酶活性的保留通过递送具有高效细胞杀伤的生物素化颗粒酶 A (b-GrA) 得到验证。该平台的模块化特性为超分子偶联和蛋白质的高效胞质递送提供了一种易于适应的策略。
2 文章亮点
1. 作者团队报告了使用生物素-链霉亲和素束缚来提供一种模块化方法来生成能够在细胞溶质中递送生物素化蛋白质的纳米载体。
2. 该策略使用链霉亲和素将生物素化蛋白质和生物素化寡(谷氨酸)肽组织成模块化复合物,然后与阳离子胍官能化聚合物进行静电自组装。
3. 形成的聚合物-蛋白质纳米复合材料证明了六种不同大小、电荷和四级结构的生物素化蛋白质货物的有效胞质递送。
4. 蛋白质功能的保留是通过递送化疗酶颗粒酶 A 来有效杀死细胞来建立的。该平台代表了一种通用的模块化方法,通过将多种成分非共价连接到单个递送载体中来进行细胞内递送。
3 图文速读
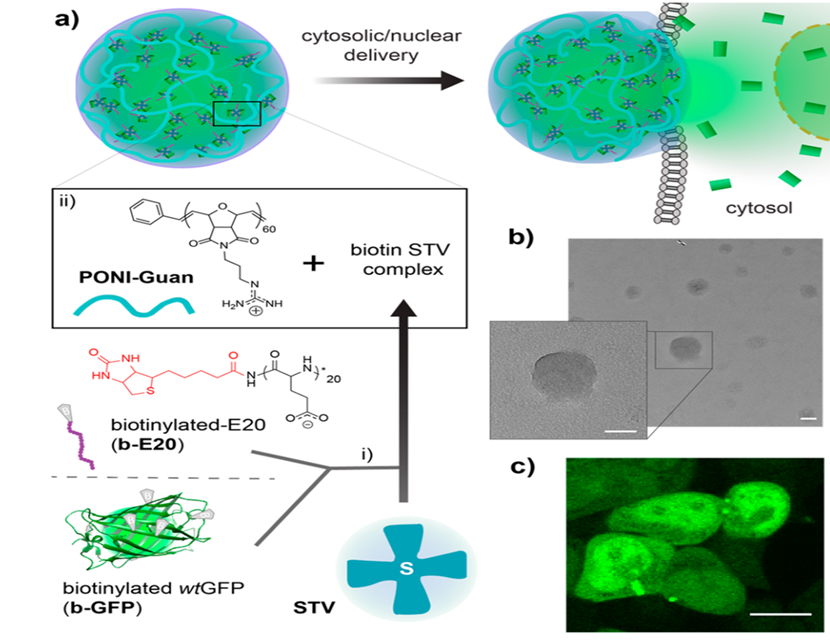
图 1. (a) 生物素化成分 b-E20 和 b-GFP 复合物 (i) 与 STV,添加 PONI-Guan 聚合物;(ii) 自组装成稳定的纳米复合材料,将蛋白质输送到细胞质;(b) PONI-Guan/b-E20/b-GFP/STV 纳米复合材料 (G/E 10) 的代表性 TEM 显微照片。比例尺 = 20 nm;(c) 共聚焦成像 (HEK-293T, G/E 10, 24 h 孵育) 显示整个细胞内有漫反射荧光。比例尺 = 10 μm。
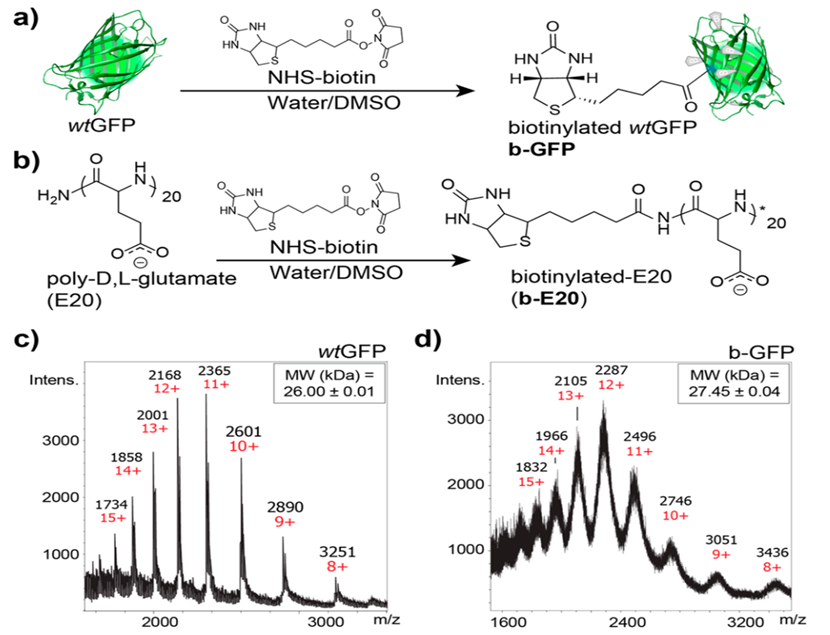
图 2. 通过 NHS 酯与 (a) wtGFP 的赖氨酸残基和 (b) E20 肽的游离末端胺偶联的蛋白质生物素化。支持信息中提供了详细信息。(c) wtGFP 和 (d) b-GFP 的代表性 ESI-MS 光谱显示质量差异。基于解卷积质量差异和相对强度估计的生物素标记残留物的平均数量(参见支持信息)。
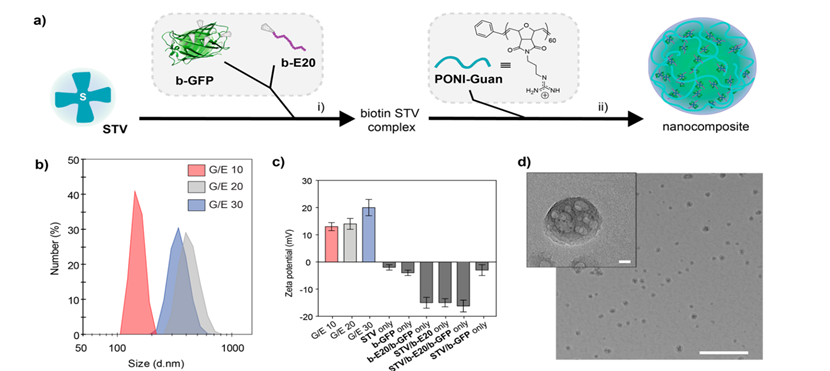
图 3.超分子纳米复合材料的表征。(a) 通过 (i) STV 与生物素化成分结合,然后 (ii) 与 PONI-Guan 均聚物复合制备纳米复合材料;(b) 代表 PONI-Guan/STV/b-E20/b-GFP(1:1:3 摩尔比,如上所述)纳米复合材料的代表性叠加 DLS 光谱,以选定的 G/E 比率配制。用数字表示的大小(按强度和体积的大小如图 S7 所示);(c) PONIguan/STV/b-E20/b-GFP 纳米复合材料在选择的 G/E 比率下的代表性 zeta 电位测量,并带有相关控制;(d) PONIguan/STV/b-E20/b-GFP 纳米复合材料的代表性 TEM 显微照片 (G/E 10)。比例尺 = 500 nm;插图比例尺 = 20 nm。
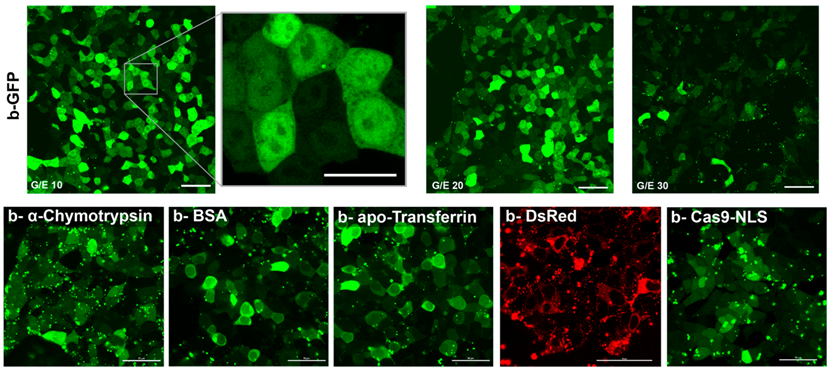
图4. HEK-293T 在孵化 24 小时后的代表性共焦图像 (10% FBS)。(顶行)选择 G/E 比率(比例尺:50 μm)的 b-GFP 递送,G/E 10 的放大图像(比例尺:20 μm)。(底行)孵育 24 小时后,)额外生物素化蛋白的细胞溶质递送。大多数传递发生在 3-5 小时内。纳米复合材料以 G/E 10 配制。比例尺:50 μm。在适当的地方发出漫射荧光和核通路信号细胞溶质通路。
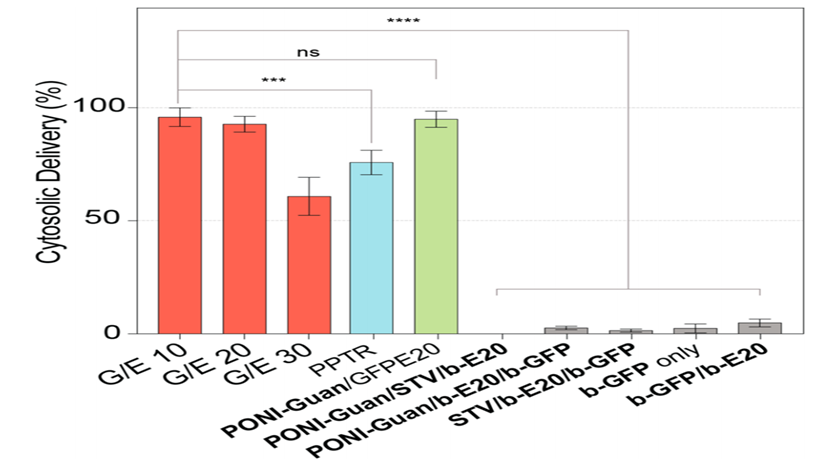
图 5. 成像流式细胞仪数据以细胞群的百分比表示,量化 GFP 的细胞溶质/核递送。如上所述,在不同的 G/E 比(红色)或各种控制条件(灰色)下配制纳米复合材料。将递送与对照进行比较:b-GFP 递送(蓝色)使用商业 Pierce 蛋白转染试剂(Thermo Scientific),在无血清培养基中孵育,以及由 PONI-Guan 在 G/E 10.41 递送的 GFP-E20(绿色)数据为六个重复孔的平均值。误差是总体的标准偏差。支持信息中提供了成像流式细胞术实验的详细信息。通过非配对 t 检验进行统计分析; *** = p < 0.001; **** = p < 0.0001; ns 不显著。
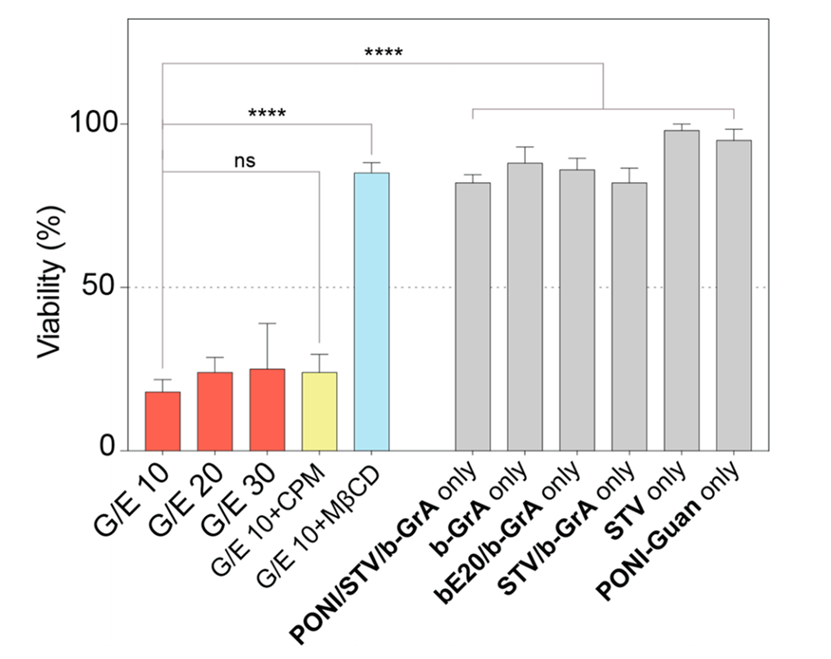
图 6. b-GrA 的传递导致细胞活力降低。由 Alamar Blue 测定的在不同条件下 PONI-Guan/STV/b-E20/b-GrA 处理后 HEK-293T 细胞的活力。G/E 10-30(红色)代表在各自的配方中使用 b-GrA 纳米复合材料进行处理。G/E 10+CPM(黄色)和 G/E 10+MβCD(蓝色)显示用小分子抑制剂试剂进行预处理的条件。对照以灰色显示。数据是六个重复孔的平均值。误差是人口的标准偏差。通过非配对t检验进行统计分析;**** = p < 0.0001; ns 不显著。支持信息中提供了详细信息。
4 总结展望
总之,作者团队通过生物素-链霉亲和素自组装提供了一种高度模块化的“即插即用”方法来有效地在细胞内递送蛋白质。生物素化固有的简单性有助于获得有效的 E-tag 递送策略,该策略使用膜融合样过程绕过内体途径。通过成像流式细胞术对生物素化 GFP 的细胞溶质递送和有效核通路进行量化,与商业蛋白质递送试剂相比,证明效率更高。该平台的扩展可容纳五种尺寸、电荷和结构不等的额外荧光蛋白货物,证明了这种生物素-链霉亲和素束缚策略用于细胞内递送的多功能性。细胞毒性蛋白颗粒酶 A 的递送提供了有效的细胞杀伤,验证了酶活性的保留和递送的治疗性蛋白的细胞溶质通路。这个模块化平台立即为离体和体外蛋白质递送提供了一种强大的方法,并为未来的体内治疗应用奠定了有希望的基础。
原文链接:https://doi.org/10.1021/acsnano.1c06768








暂无评论
发表评论