2021年5月30日,中国工程院院士钟南山在中国科学技术协会第十次全国代表大会上提到:到今天为止,中国的疫苗在将近二十多个国家中没有出现重大事故。中国的疫苗是比较安全的。然而中国疫苗的接种率还是很落后,仅包括接种一针的民众,全国新冠疫苗的覆盖率约在40%。希望在今年年底全国新冠疫苗覆盖率争取达到80%。据国家卫建委通报数据显示,截至北京时间2021年5月30日,31省(自治区)和新疆生产建设兵团累计报告接种新冠病毒疫苗63917.2万剂次。

图1. 钟南山院士在中国科学技术协会第十次全国代表大会上讲话(中国青年报)
世界卫生组织(WHO)早前宣布(2021年5月7日),中国国药集团的一款COVID-19疫苗列入世界卫生组织“紧急使用清单(emergency use listing, EUL)”,为该疫苗在全球推广使用打开了绿灯。这款由中国生物技术集团公司旗下的北京生物制品研究所生产的疫苗,成为列入世界卫生组织紧急使用清单的第六款疫苗。

世卫组织的“紧急使用清单”是新冠肺炎疫苗实施计划(COVAX)计划疫苗供应的一个先决条件,这必须对COVID-19疫苗的质量、安全性和有效性、风险管理计划和方案适用性等多方面进行综合评估。而根据世卫组织的标准,有效率为50%以上,最好接近或高于70%,并且安全性良好的新冠疫苗才能列入紧急使用清单。我国国药集团研制的COVID-19疫苗被列入世卫组织“紧急使用清单”,一方面证实了这款COVID-19疫苗的安全性和有效性符合国际标准,全球没有疫苗生产能力的国家都可以放心接种使用,不用担心质量问题;另一方面也必将增强相关国家药品监管机构批准这款疫苗的信心,加快国药集团疫苗进口和接种速度。
世卫组织对国药疫苗评估报告

图2. 中国生物技术集团(CNBG)、国药集团(Sinopharm)研发的新型冠状病毒灭活疫苗BIBP的使用临时建议
免疫战略咨询专家组(SAGE)是世卫组织在疫苗和免疫方面的主要咨询小组,目前SAGE已经发布针对辉瑞疫苗(2021年1月8日)、莫德纳疫苗(2021年1月25日)、阿斯利康疫苗(2021年4月21日)和杨森COVID-19疫苗(2021年3月17日)的接种建议,并且出台了疫苗获取框架和人群接种优先排序路线图。在2021年5月7日,SAGE公布了中国国药集团研制疫苗的接种使用建议,同时也公布对国药疫苗的评估报告。
世卫组织对国药疫苗进行安全性、免疫原性和有效性三大类临床试验数据进行清楚分类,对应的人数也按照年龄在18~59岁之间和60岁以上进行分类。这里对免疫原性进行解释下:免疫原性,就是抗体转阳率、中和抗体滴度一类的结果,是审查疫苗是否引起人体免疫反应以及诱发的免疫反应有多大。评估一种疫苗时,免疫原性好,比如抗体转阳率100%、诱发抗体滴度高等,是疫苗有效性的必要条件。
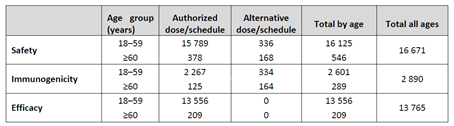
图3. 截至2021年4月20日,至少接种一剂COVID-19疫苗BIBP的临床试验总人数
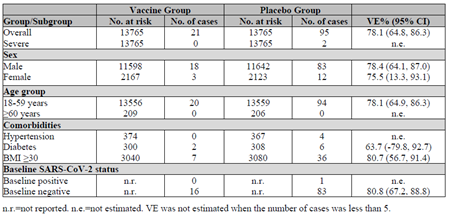
图4. 截至2020年12月30日数据,国药疫苗的防护有效数据统计
从在阿联酋、巴林、埃及、约旦等国家进行的三期临床实验数据结果显示,国药疫苗对病毒感染所致疾病的保护效率为78.1%,置信区间在64.8%~86.3%。同时疫苗的安全性良好,临床试验数据中没有发现安全问题。总体上,国药新冠疫苗的安全性和有效性表现还是很不错的。
“紧急使用清单”内的疫苗的信息对比
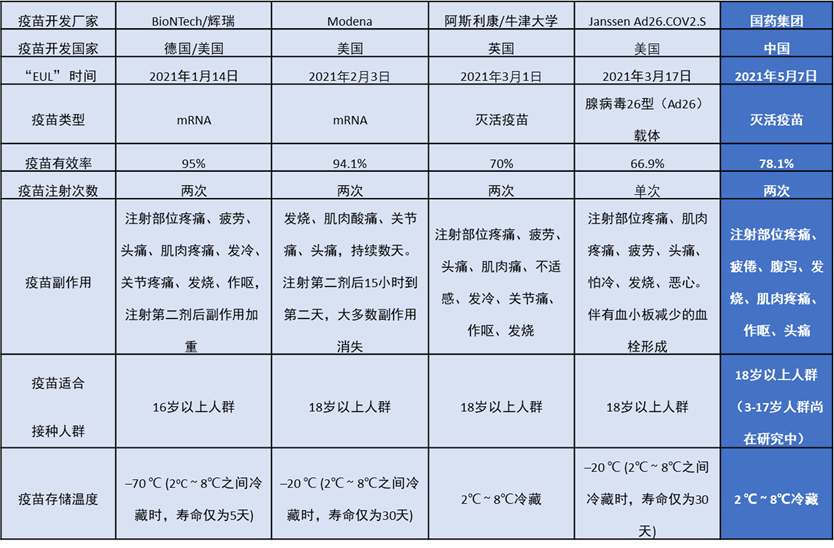
BioNTech/辉瑞疫苗已经在美国上市,同时疫苗有效率为95%,Modena的COVID-19疫苗有效率也能达到94.1%。也就是说,以前没有感染过新冠病毒的人群,在完成两剂疫苗接种之后,有近95%的可能性免于感染新冠病毒。而我国国药集团研制的灭活病毒疫苗(Vero 细胞)只有78.1%的有效率,在有效率方面确实没有国外疫苗高,但是已经达到世卫组织的制定的标准:可接受新冠疫苗的有效性为50%,最好能达到70%和以上的标准。同时评价一种疫苗不能仅看有效率这一方面,对于评估疫苗好不好,需要综合评估。疫苗的安全性和有效性是主要因素,同时对于疫苗研发的难度以及产能等方面也需要考虑。对于安全性的考究,针对目前已公布的数据显示,国内灭活病毒疫苗都没有出现严重不良反应,或已经发生的不良反应程度均较轻,例如疲倦、发烧、肌肉疼痛等一般都能自行恢复。
疫苗是一种生物制品,那么就需要保证生物制品的质量,则必须要在规定的冷链状态下存储、运输,COVID-19疫苗也不能例外。从存储温度来看,国外的BioNTech/辉瑞和Modena疫苗的存储温度要求非常严格,BioNTech/辉瑞疫苗需要存储在在–70℃ 苛刻条件下,在2℃~ 8℃之间冷藏时,寿命仅为5天;Modena疫苗需要存储在在–20℃ 环境下,在2℃ ~ 8℃之间冷藏时,寿命为30天。而国药集团研制的灭活病毒疫苗可以存储在2℃ ~ 8℃环境下,普通冰箱就能满足存储的要求,这极大拓宽了灭活病毒疫苗的广泛接种的可能,具有极强的可普及性,对于阻止新冠病毒的大范围传播也将做出巨大贡献。
我国新冠灭活疫苗(Vero 细胞)“诞生记”
目前我国国内新冠疫苗接种工作正在稳步有序的推进,那么一剂“中国制造”的新冠灭活病毒疫苗,需要经过怎样的生产流程才能被群众接种使用呢?
图5. 国药集团中国生物新冠灭活疫苗(Vero 细胞)
一支灭活疫苗的生产和检定全流程需要耗费40多天,经过细胞培养、病毒培养、灭活、纯化、配比(半成品)、罐装、包装等七大流程,但是每个流程中又包含许多细节步骤。其中至关重要的病毒灭活工艺要求相当严格,必须在P3(三级生物安全水平)生物医药生产车间进行;在新冠疫苗罐装之前,需要对存储的西林瓶进行洗瓶和高温消毒操作;在包装过程中,疫苗需要经过灯检,观察是否存在含有颗粒、异物和玻璃渣等不合格的产品。最后合格的产品才能进一步被包装使用,而国药疫苗包装是也是第一种带有疫苗瓶监控器的新冠疫苗,疫苗瓶上的小标签会随温度而变色,从而卫生工作者可以清晰获知疫苗是否可以安全使用。另外在同步进行的还有对疫苗进行贯穿全程的质控检测,以保证疫苗产品的质量和安全。
接种新冠疫苗,共筑免疫长城
新冠疫苗接种是非常有必要的。一方面,我国几乎所有人都没有针对新冠病毒的免疫力,面对新冠病毒我们是非常脆弱的。在感染病毒之后,部分人群的生命会受到威胁,甚至造成死亡。另一方面,接种新冠疫苗是每个公民的责任和义务。我们辛苦取得的防疫优势是需要注射疫苗来进一步巩固。只有在注射疫苗之后,大部分人群可以获得免疫力,从而逐渐在人群中建立免疫屏障,进一步才能有效阻隔新冠肺炎的流行。







暂无评论
发表评论