要点速览
1. 生物固氮酶的多金属硫骨架催化位点可以在常规条件下将二氮(N2)有效转化为氨 (NH3)。受生物固氮酶的启发,作者通过 FeWO4 纳米颗粒表面的硫取代合成了一种双金属硫化物材料(FeWSx@FeWO4)作为高效的N2还原(NRR)催化剂。
2. 由此制备的FeWSx@FeWO4催化剂表现出相对较高的NH3产率,为30.2 mg h-1 mgcat-1。在-0.45 V vsRHE 电压下,该催化剂在流动池中的法拉第效率为16.4%;
3.原位拉曼光谱和肼还原动力学分析表明,未解离的肼中间体(M-NH2-NH2)在双金属硫化物催化剂表面的还原是 NRR的速率决定步骤。因此,这项工作可以为阐明NRR催化剂构效关系提供新的方向。
图文速读
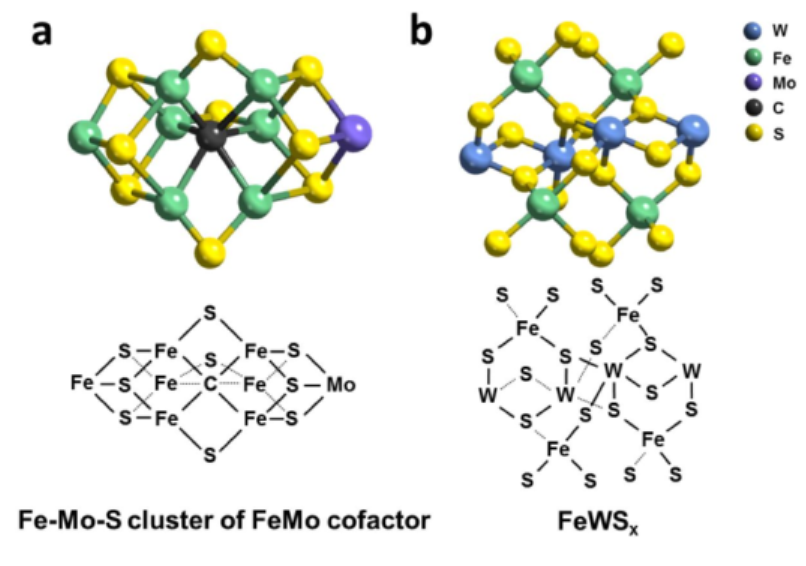
示意图 1:a)固氮酶中的Fe-Mo-S团簇,和b)FeWSx@FeWO4NPs表面合成的FeWSx的结构。
双金属的结构(示意图 1a)可以为设计高效的人工 NRR 催化剂和对氮加氢过程的机理提供指导。在此,受固氮酶双金属硫结构的启发,作者通过 FeWO4 纳米颗粒表面的硫取代合成了铁钨双金属硫化物催化剂(FeWSx@FeWO4,示意图 1b)。
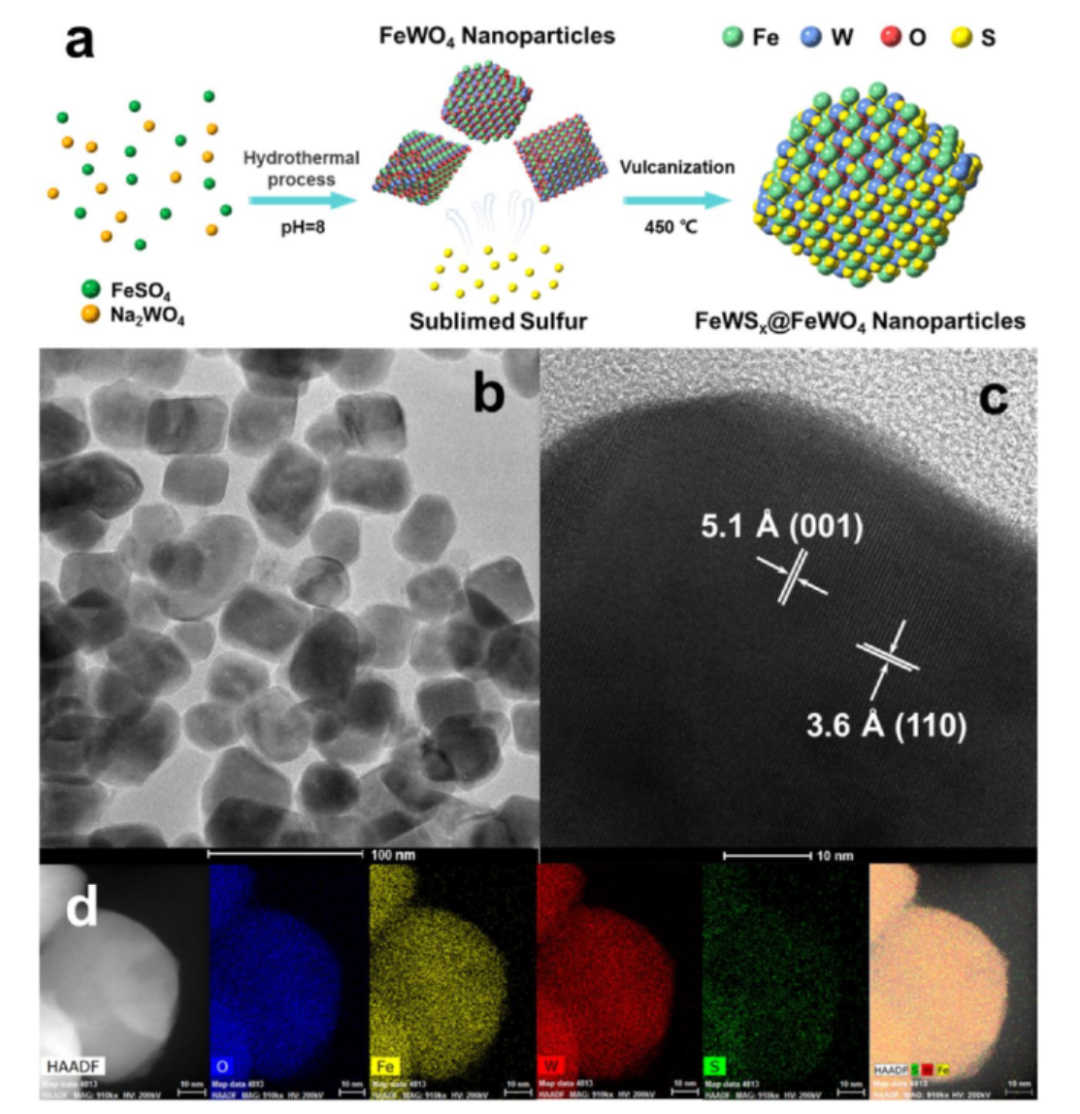
图 1. a) FeWSx@FeWO4 纳米粒子 (NPs) 的合成过程示意图。FeWSx@FeWO4NPs 的b) TEM 和 c) HRTEM 图像。 d) FeWSx@FeWO4 NPs 的HAADF-STEM 和相应的EDX元素mapping图。
如图 1a 所示,FeWSx@FeWO4 纳米颗粒(NPs)是使用两步制造策略合成。首先通过水热反应制备了 FeWO4 NPs,然后,在 450 °C 的氩气气氛下FeWO4NPs 的表面氧被硫原子取代。根据 TEM 图像(图 1b),FeWSx@FeWO4-2样品的直径约为50±10 nm。高分辨率 TEM 图像(图 1c)显示了晶格间距为5.1 Å 和 3.6 Å,对应于 FeWO4的 (001) 和 (110) 晶面。EDX mapping图像显示了 Fe、W、S 和 O 在FeWSx@FeWO4 纳米颗粒中均匀分布(图 1d)。
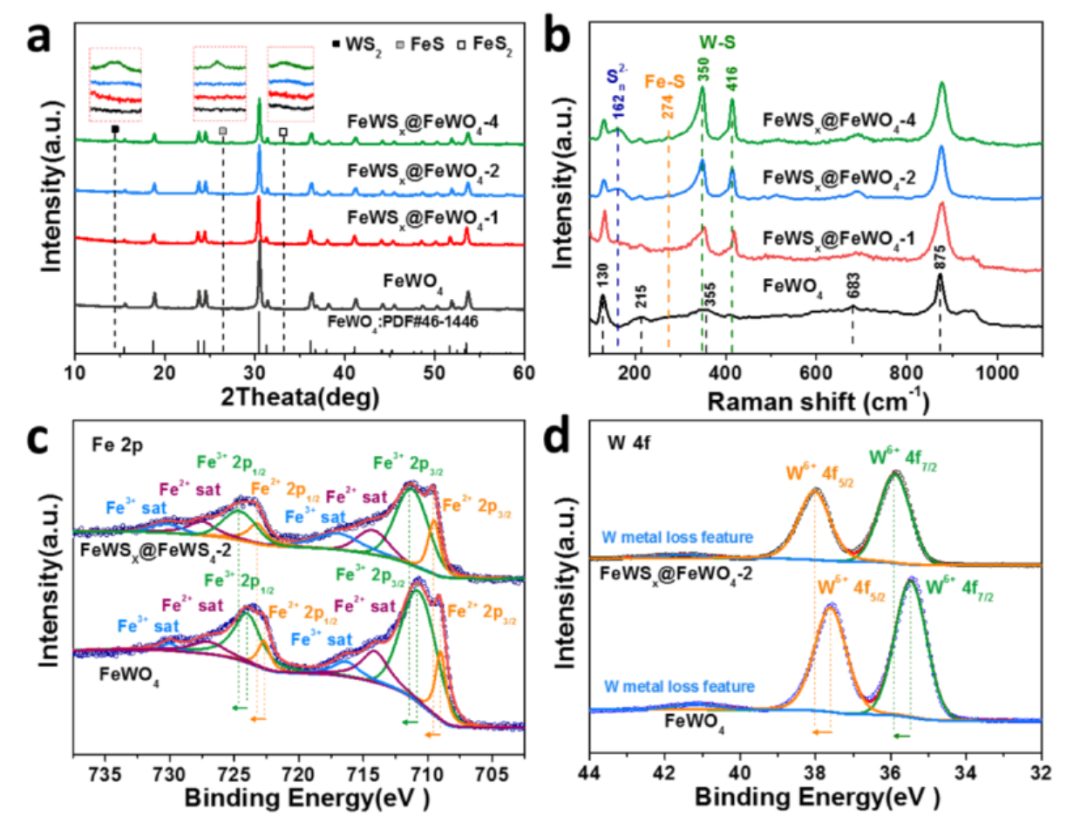
图 2. FeWO4 和 FeWSx@FeWO4的a) XRD 图和 b)拉曼光谱。FeWO4 和 FeWSx@FeWO4-2 NP 的c) Fe 2p 和 d) W 4f 的 XPS光谱。
FeWSx@FeWO4和 FeWO4 的 XRD 图案(图2a)表明在 18.8°、30.5°、36.3°、41.2° 和 53.7° 处的衍射峰可以分别归为FeWO4 的(100),(111)、(021)、(121) 和 (221) 晶面。硫化后,Sn2- (162 cm-1)、Fe-S (274 cm-1)、和 W-S (350 和 416 cm-1)的拉曼峰可以被测得,且这些拉曼峰的强度随着硫化过程中硫的量增加而增加(图2b)。FeWO4 的 Fe 2p 高分辨率 XPS 光谱可以分为四组峰,分别归因于 Fe2+ (722.7 eV 和 709.1 eV ) 和 Fe3+(724.1 eV 和710.8 eV )及其卫星峰信号(730.0 eV、727.1 eV、716.4 eV 和 714.1 eV)(图 2c)。W 4f XPS光谱的峰位分析表明 W 存在 +6 价态(4f5/2, 37.6 eV 和 4f7/2,35.5 eV) (图 2d)。
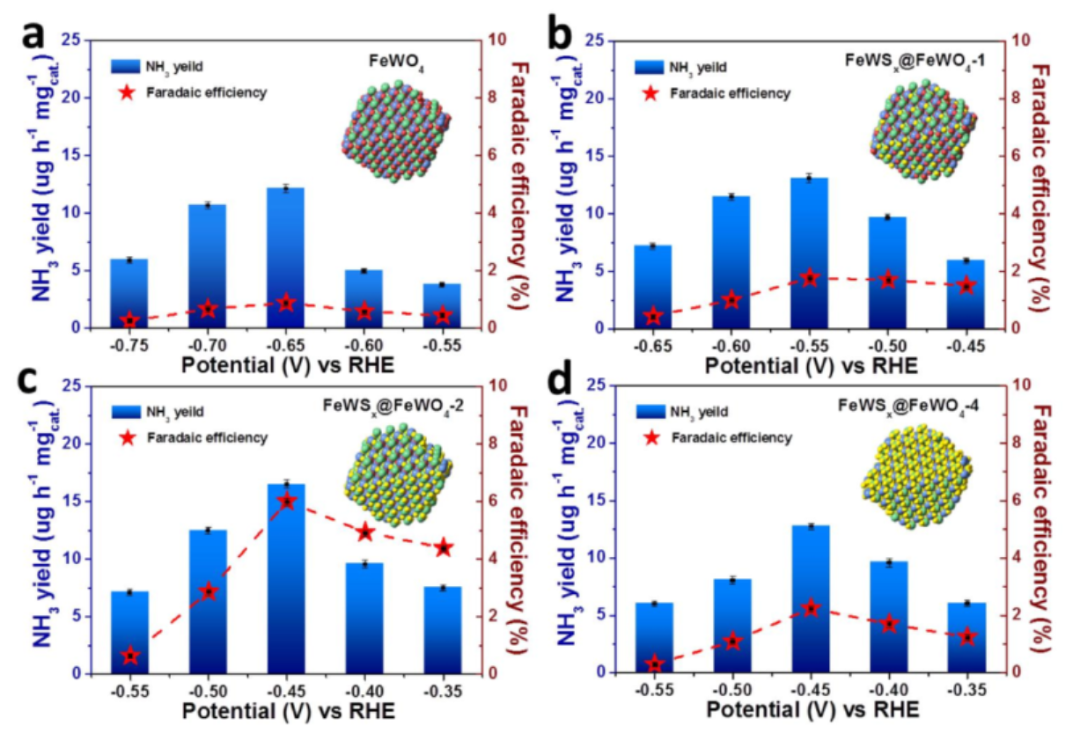
图 3. a) FeWO4, b) FeWSx@FeWO4-1,c) FeWSx@FeWO4-2 和 d) FeWSx@FeWO4-4在不同电位下的氨产率和法拉第效率。
在 -0.65 V(vs. RHE)时,FeWO4 表现出的最高 rNH3 和 FE,为 12.26 mg h-1 mgcat-1和 0.89%(图 3a)。硫化后(图 3b 和3c),FeWSx@FeWO4-1和 FeWSx@FeWO4-2 的最高活性电位正向偏移了,这与 LSV 结果一致。FeWSx@FeWO4-1的rNH3最高为13.19 mg h-1 mgcat-1,FE 最高为 1.5%。FeWSx@FeWO4-2的rNH3最高为16.6 mg h-1 mgcat-1,FE 最高为 6.01%。FeWSx@FeWO4-4的rNH3最高为12.88 mg h-1mgcat-1,FE 最高为 2.2% (图3d)。
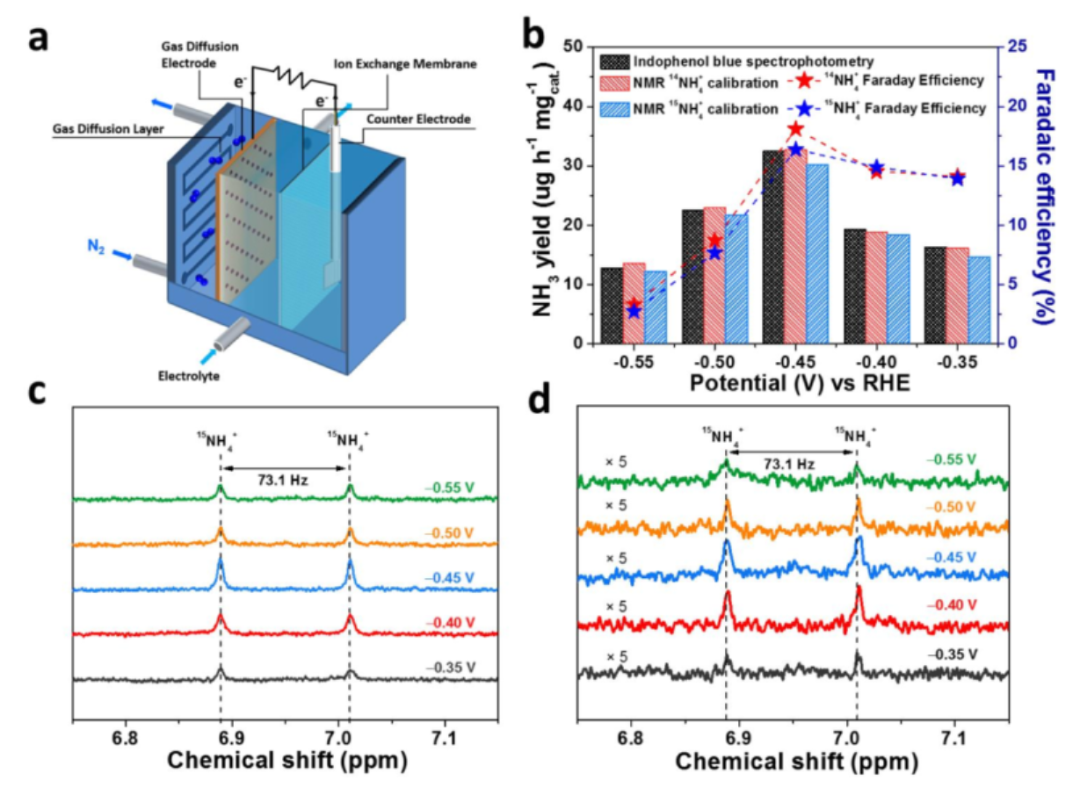
图 4. a) NRR 的流动池示意图。 b) 氨产率和15N2活性测试的法拉第效率。c) 电解质和 d) 气体吸收液中 15NH4+ 的 1H-NMR 光谱。
为了进一步提高NRR效率,1 mg FeWSx@FeWO4-2 催化剂被沉积在气体扩散电极上(气体扩散层,GDL,1 cm2),并在流通池中重新测量其性能(图 4a)。FeWSx@FeWO4-2的rNH3最高为32.7 mg h-1 mgcat-1,FE 最高为 18.1% (图4b)。电解质(图4c)和气体吸收液(图 4d)的1H NMR谱显示出耦合常数为 73 Hz的双峰,与 15NH4+ 的标准峰匹配良好,从而有力地支持了这样一个事实,即 NH3 的产生是由 N2 还原得到。
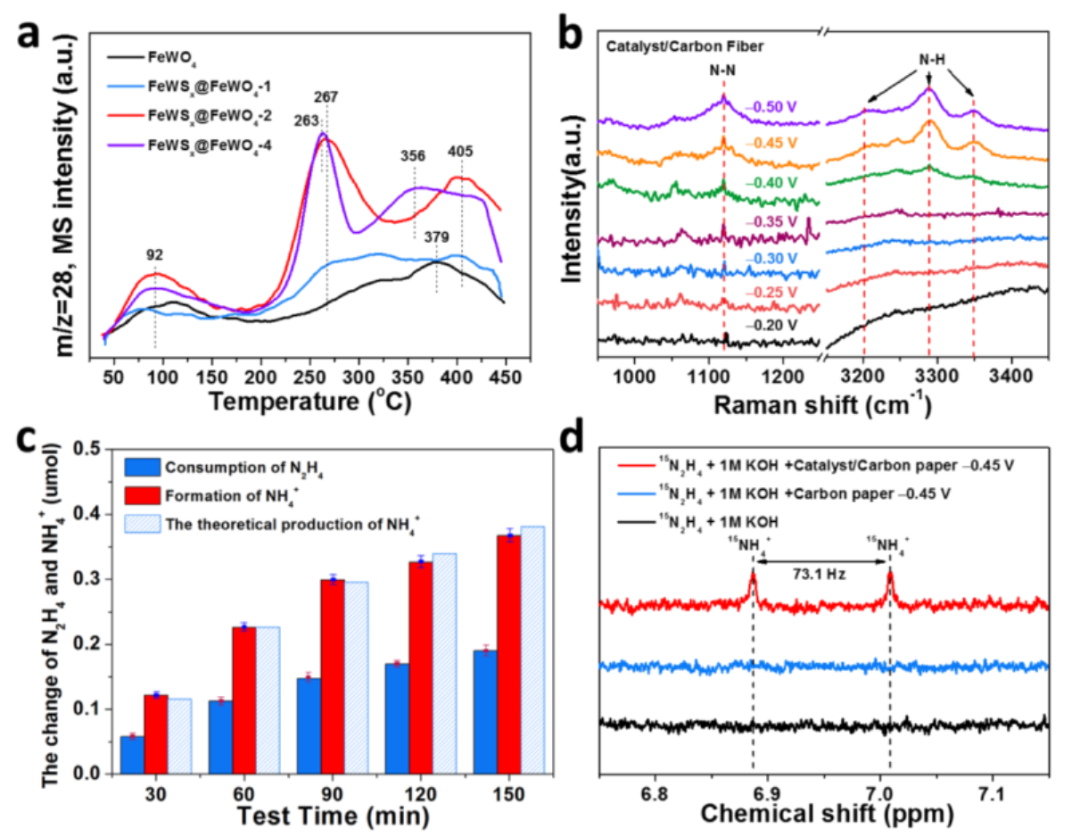
图 5. a) FeWO4 和 FeWSx@FeWO4催化剂的 N2-TPD 曲线。 b) FeWSx@FeWO4-2电化学原位拉曼光谱。 c) 肼的消耗,氨的形成,以及不同反应时间下氨的理论产量的比较。 d) 在含有15N2H4的 1 M KOH 溶液中测试后,得到的电解液的1H-NMR 谱。
如图所示, N2 程序升温脱附(N2-TPD)曲线中(图 5a),所有样品都在 50-175 °C 范围内出现峰值,这可以归因于 N2 的物理吸附。如图 5b 所示,当电位达到 -0.4 V vs RHE时,1119、3207、3288 和 3349 cm-1的振动带可以被观察到,这归因于 N-N 的拉伸模式和 N-H 物种。重要的是,NH3的产生量几乎是肼消耗量的两倍(图 5c),表明FeWSx@FeWO4-2表面上的肼分解过程实际上是将一个肼分子还原成两个NH3分子,而不是歧化反应。如图 5d 所示,以 15N-硫酸肼 (15N2H6SO4)为原料电解后的吸收液显示出一个特征双峰(偶联常数73.1 赫兹);然而,在对照实验中无法检测到 15NH4+,这证实NH3的产生来自于肼中间体的 N-N 键断裂反应。
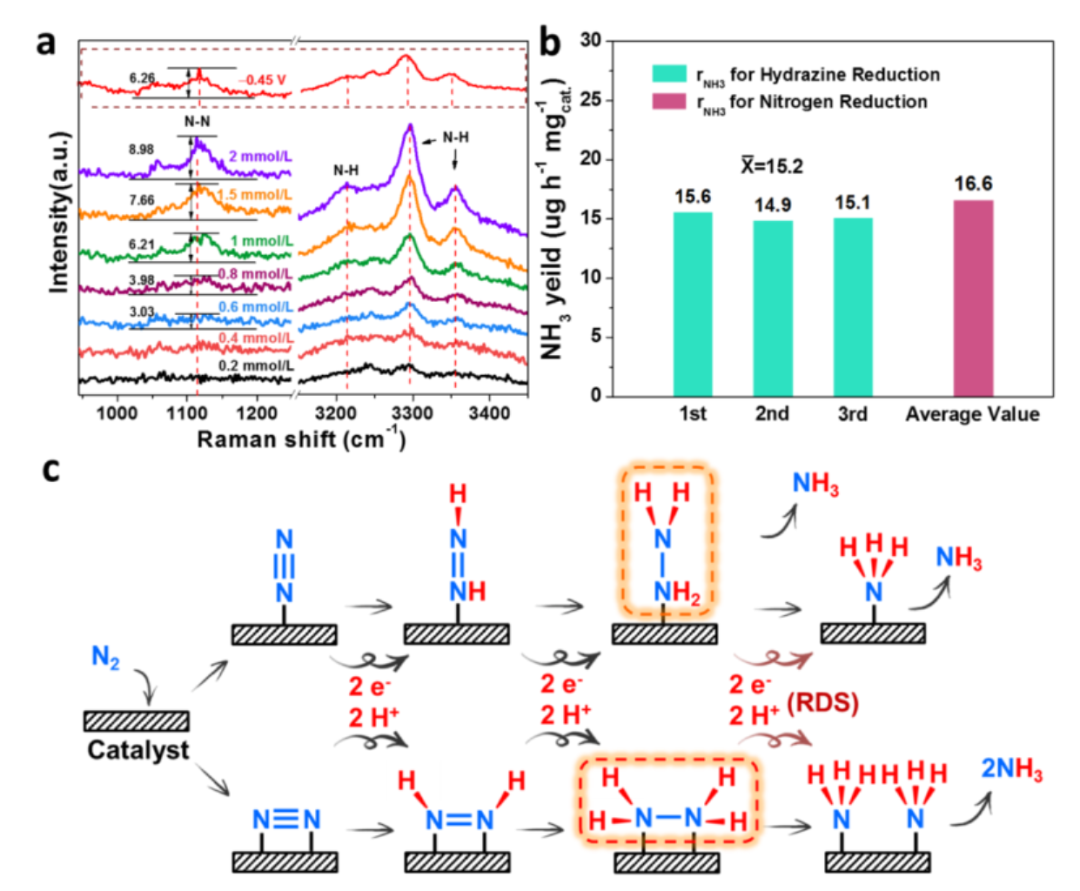
图 6. a) 不同浓度肼溶液 (1 M KOH)中的电化学原位拉曼光谱。 b) 在 1 mmol/L 肼溶液(1 M KOH,@-0.45 V,FeWSx@FeWO4-2 作为催化剂)中的氨产率。 c)FeWSx@FeWO4-2催化剂上N2还原为NH3的途径示意图。
图6a拉曼光谱中,1114 cm-1 处的特征峰对应于 N-N键振动,证明了催化剂表面的肼过渡态。在 -0.45V 下,肼还原的rNH3 为 15.2 mg h-1 mgcat-1,与 N2还原的结果一致(-0.45 V 时为 16.6 mg h-1 mgcat-1),表明表面未解离的肼类物种的还原是FeWSx@FeWO4-2上电化学 NRR 的决速步骤。因此,作者图 6c 中提出了FeWSx@FeWO4-2 催化剂上可能的NRR 加氢机制。







暂无评论
发表评论