1引言
免疫检查点阻断(ICB)疗法是新兴的癌症免疫疗法之一。比如,阻止T淋巴细胞上的程序性细胞死亡蛋白1(PD1)与癌细胞和抗原呈递细胞(APCs)上的程序性死亡配体1(PDL1)结合,从而在不同类型的癌症中引起有效的临床治疗反应。然而这种方法面临着很多问题,如作为靶标的细胞标记物并不只在癌细胞上表达,在正常细胞上也以低水平表达。此外,靶细胞和正常细胞之间内源性受体群体的微小差异不能提供高选择性和诱导低客观反应率。因此,抗程序性死亡(抗PD1或抗PDL1)治疗的反应虽然显著,但仍然局限于一小部分患者,在ICB治疗中也经常出现非目标效应和毒性等副作用。
考虑到癌症和正常细胞之间内源性受体群体的微小差异,可以利用活细胞上的多个标记,用逻辑门反应来进行识别。近些年,几种基于逻辑的方法被开发来针对多个生物标记,包括双特异性抗体,逻辑门控DNA机器人、适配体DNA纳米爪等。适配体,通常被称为“化学抗体”,是单链DNA或RNA寡聚物,其被用于感知、处理和响应复杂的细胞环境等领域,具有高度的特异性、可编程性和生物计算能力等优点。然而,与抗PDL/PDL1抗体一样,这种抗PDL/PDL1适配体的客观反应速率也很有限。
2课题设计
谭蔚泓院士课题组认为,通过引入基于适配体的逻辑运算反应可以提高ICB的相关治疗效率和功效。因此,他们利用抗PDL1的适配体识别和基于环辛炔/叠氮基的生物正交反应,提出了一种基于适配体的逻辑计算反应,通过对细胞表面的抗PDL1适配体进行化学修饰来实现有效和持续的免疫检查点阻断治疗。他们将二苯并环辛炔(DBCO)与适体的5'端偶联,将叠氮化物作为“化学受体”掺入细胞表面糖蛋白中,引起了二苯并环辛炔连接的抗PDL1适配体(D-aPDL1)在活癌细胞上的基于逻辑的选择性和共价修饰,并长期保留,通过阻断PD1-PDL1信号通路提高临床癌症治疗的治疗效率和精确度。抗PDL1适配体可以识别肿瘤细胞表面表达的PDL1,然后通过基于逻辑计算的生物正交反应与B16F10细胞上叠氮标记的糖蛋白共价共轭,显著提高治疗效率和降低副作用。(图1)
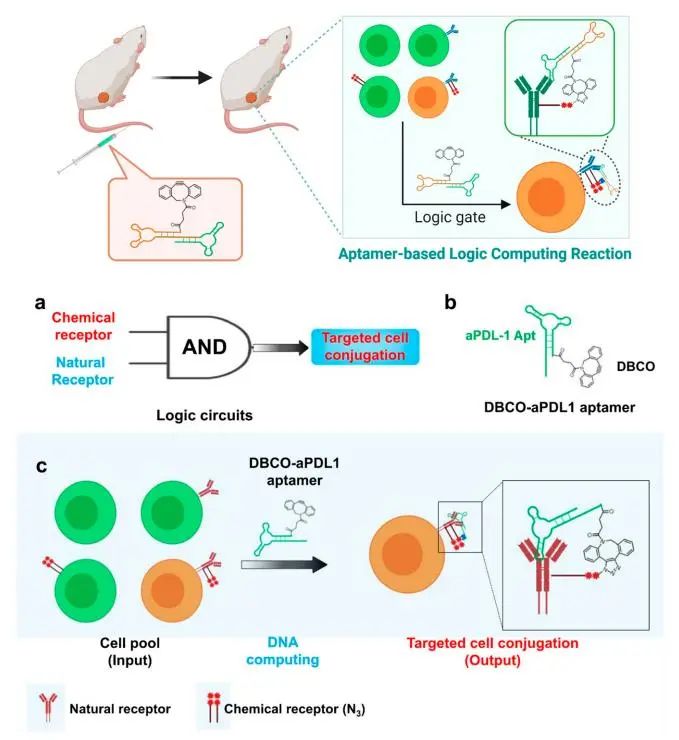
图1 (a)目标细胞上适聚体特定共轭的“与”逻辑门反应的一般原理 (b)DBCO-aPDL1适配体的结构 (c)基于逻辑门反应的活细胞精确治疗癌症的反应方案
3研究结果
经过验证叠氮糖蛋白在活细胞表面作为化学受体的标记表达能力后,团队用D-sgc8适配体验证了在细胞表面构建基于适配体和环辛炔生物正交化学的逻辑门反应可能性。D-sgc8适配体可以专门识别CCRF-CEM细胞表面的蛋白酪氨酸激酶7(PTK7),从而可以通过共聚焦成像直观地观察到适配体结合的能力。共聚焦显微镜和流式细胞术结果共同表明,Ramos细胞缺乏PTK7激酶,因此在Ramos细胞中没有观察到明显的荧光信号,甚至在叠氮标记的Ramos细胞中也没有观察到明显的荧光信号。
而在含有PTK7的CCRF-CEM细胞中,只有当PTK7和含氮糖蛋白受体都存在于细胞表面(即含氮CCRF-CEM细胞)时,D-sgc8-FITC适配体才能在细胞表面共轭(图2b,2c)。抗PDL-1适配体也表现出了同样的结果,只有当INF-γ和Ac4ManNAz共同作用于B16F10细胞时,细胞才会被标记点亮(图3b,3c)。INF-γ在其中起到了促进癌细胞过表达PDL1受体的作用,Ac4ManNAz则令细胞能够在表面糖蛋白上表达出叠氮基团。随后,团队又发现在体内实体瘤中引入叠氮标记,同样会导致适配体结合的准确程度和持续时间的增加(图3e)。
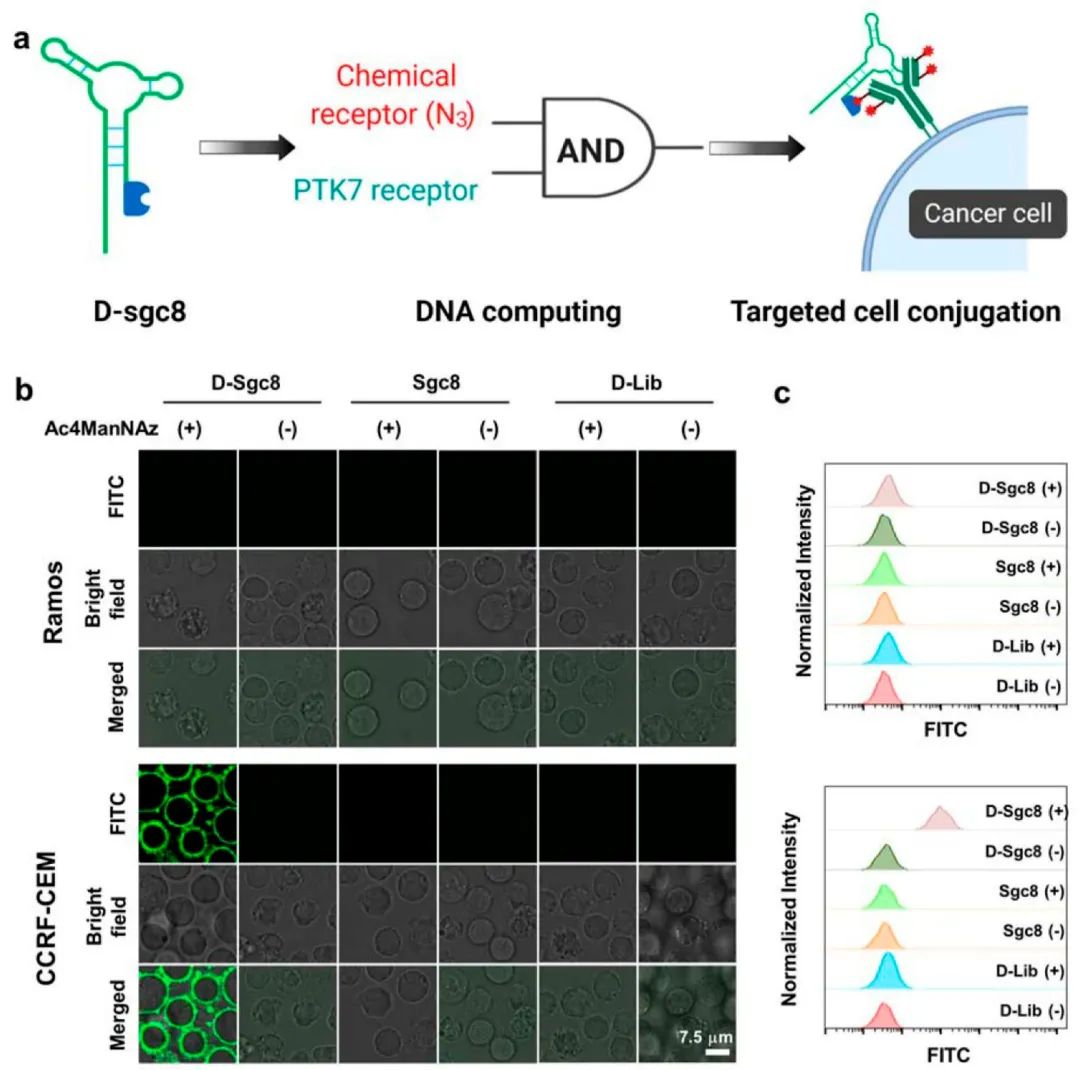
图2 利用D-sgc8适配体在活细胞表面构造逻辑门反应 (a)基于D-sgc8适配体和环辛炔点击化学构建的逻辑门反应示意图;(b)共聚焦显微镜和(c)流式细胞术结果显示,只有当D-sgc8适配体和叠氮标记的糖蛋白共同表达在细胞表面时,D-sgc8-FITC适配体才能在细胞表面共轭。
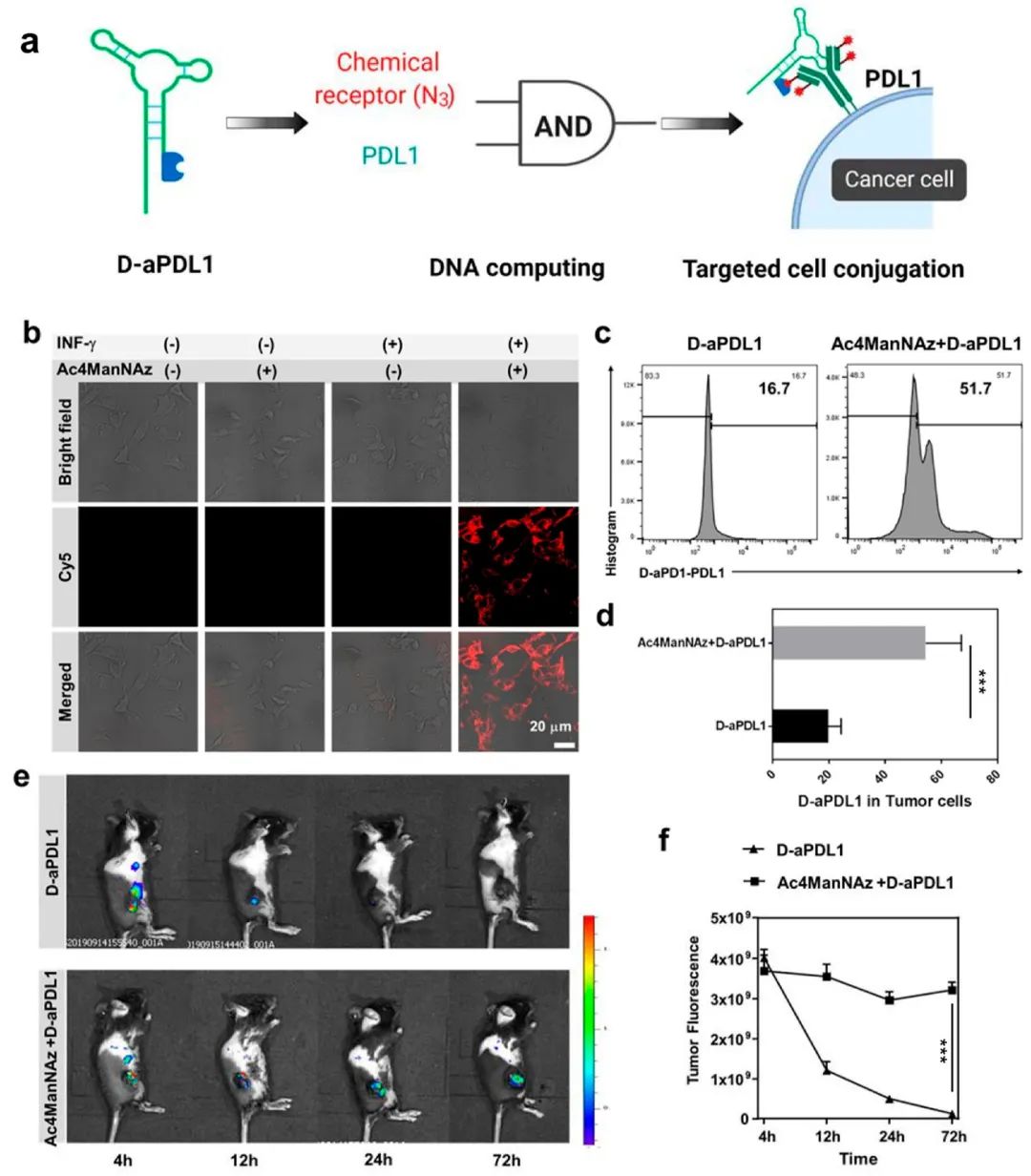
图3 利用D-aPDL1适配体在活癌细胞表面构造逻辑门反应 (a)基于D-aPDL1适配体和环辛炔点击化学构建的逻辑门反应示意图;(b)共聚焦显微镜和(c)流式细胞术结果显示,只有当D-aPDL1适配体和叠氮标记的糖蛋白共同表达在细胞表面时,Cy5荧光才能在细胞表面显著增强;(e)注射D-aPDL1后,是否表达Ac4ManNAz小鼠的体内荧光图像。
验证了基于D-aPDL1和环辛炔的逻辑门反应在细胞表面共轭标记的能力后,团队在体内验证了该反应用于体内精确检查点阻断免疫疗法的效果。对于荷瘤小鼠的治疗分组情况如图4a所示,通过对比各实验组小鼠的肿瘤体积和生存期,可以发现,当D-aPDL1适配体和Ac4ManNAz共同作用时,小鼠的肿瘤体积和存活率得到了较好的抑制。因此,由于“与”逻辑计算反应中环辛炔生物正交化学的加入,D-aPDL1适配体可以实现精确和长期的检查点阻断免疫治疗。(图4)
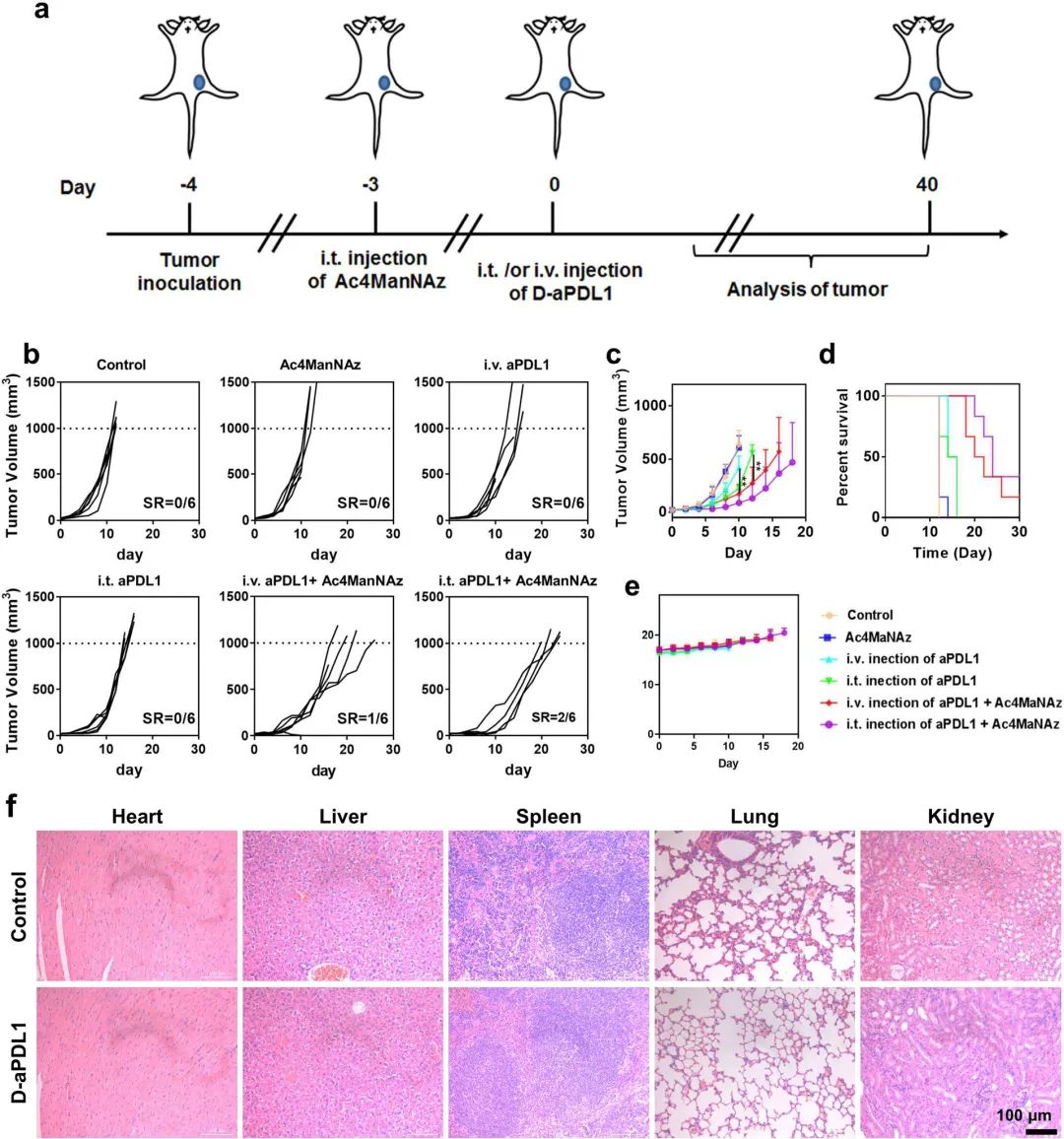
图4 基于D-aPDL1适配体和环辛炔生物正交化学的逻辑门反应用于体内精确的检查点阻断免疫治疗
最后,团队衡量了D-aPDL1适配体引发的t细胞介导的免疫反应。用流式细胞术分析了肿瘤浸润淋巴细胞的情况。D-aPDL1适配体和Ac4ManNAz共同作用后,CD3+ 和CD8+ T细胞比例比起D-aPDL1适配体单独作用都有显著的增加。同样地,与效应子T细胞增殖和生长密切相关的细胞周期相关蛋白(Ki67)的表达在D-aPDL1适配体和Ac4ManNAz共同作用后要高得多。颗粒酶B(GrazB)是一种主要的效应分子,作为CTL激活的特征,在CD8+T细胞被刺激并分化为细胞毒性T淋巴细胞时表达,也有着高表达水平。此外,比起D-aPDL1适配体单独作用,一些细胞因子分泌数量也有显著增加。(图5)
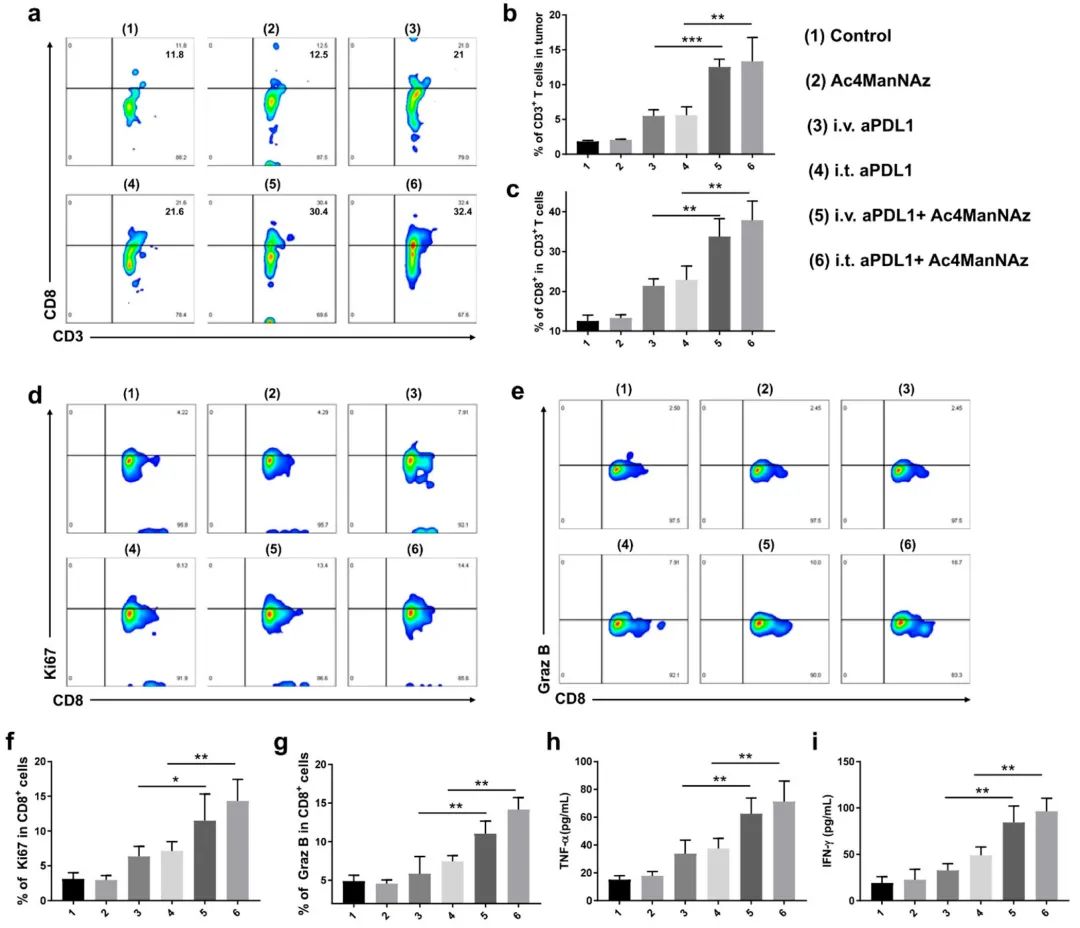
图5 流式细胞术结果,验证在D-aPDL1适配体和Ac4ManNAz共同作用后引起体内抗肿瘤免疫反应的显著增强。
4总结
总的来说,该团队设计了一种简单而通用的策略,通过操纵逻辑门反应来选择性识别和缀合治疗性D-aPDL1、D-sgc8-PA和D-sgc8-99mTc等适体,以提高抗癌治疗的治疗效率和精度。通过将叠氮化物作为“化学受体”,允许癌细胞与D-aPDL1适配体发生更高效和特异性的共价反应,从而显著延长小鼠的整体存活率。这种新型的,通过逻辑门反应耦合多种受体克服癌症和正常细胞之间内源性受体群体的微小差异的方法,为后续的肿瘤特异性靶向治疗研究提供了新的思路。
原文链接:
https://pubs.acs.org/doi/10.1021/jacs.1c02016
DOI:10.1021/jacs.1c02016.





暂无评论
发表评论