01
研究背景
电化学水分解制氢技术可为能源的可持续发展和解决环境问题提供新的方案,因而在近些年引起了人们的广泛关注。其中,贵金属基单原子催化剂(PMSACs)由于其最大的原子利用率和独特的电子结构,可在减少金属负载量的同时保持较高的催化性能,被广泛应用于水分解催化。
02
工作介绍
北京大学郭少军教授团队总结了具有优异性能的贵金属单原子催化剂在电化学水分解催化领域的最新研究进展。首先对PMSACs的合成策略进行了分类和介绍,然后,介绍了SACs的表征技术,最后,对开发适用于电化学水分解应用的新型贵金属单原子催化剂所面临的主要挑战和机遇进行了总结与展望。该工作以“Recent progress on precious metal single atom materials for water splitting catalysis”为题发表在SusMat期刊上(DOI: 10.1002/sus2.15)
03
作者介绍

郭少军 教授
郭少军教授长期致力于将国家重大需求与基础研究相结合,重点研究燃料电池、氢能与储能电池。发展了高性能原子、亚纳米和纳米催化材料设计的思想,提出了材料应变调控催化的新方式,率先揭示了材料本征拉应变和双轴应变调控催化材料电子结构与催化性能的化学机制,研制出了系列新概念电/光催化材料,显著提升了燃料电池和氢能催化性能,解决了能源小分子反应动力学慢的关键难题,有力推动了材料、化学和能源的交叉与融合。独立工作后以通讯作者在Nature、Science、CNS系列(17)、Adv. Mater.(28)和Angew. Chem.(11)等高水平期刊(IF>10)发表论文150余篇,所发论文被引4万余次,h指数110,连续七年入选“全球高被引科学家”榜单。荣获首届科学探索奖、中国青年科技奖、茅以升北京青年科技奖和中国化学会-英国皇家化学会青年化学奖。(曾)主持国家杰出青年基金、科技部重点研发计划、首届北京杰出青年基金和奥本海默杰出学者基金等。Chem. Commun.、Sci. Bull.、Sci. China Mater.、eScience等10余种杂志的(顾问)编委。受邀成为VinFuture Prize、Japanese Prize及Xplorer奖的提名专家。
上下滑动查看全部
04
主要内容
1.合成方法
通过自下而上和自上而下的方法,已经发展了一些广泛应用的方法来合成PMSACs。本文综述了几种主流的合成SACs的方法,包括高温热解法、电化学和光化学还原法、湿化学法等。
1.1 高温热解
高温热解是一种较普遍的制备SACs的方法。通过在惰性或腐蚀性气氛(如 Ar、N2、NH3和PH3)中在适当温度下热分解某些前驱体,可合成原子水平分散的单原子催化剂。其中,合成前驱体包括金属有机骨架(MOF)、聚合物、石墨烯、碳纳米管、金属大分子复合物和过渡金属化合物等。基本上,这些前驱体都具有多孔骨架结构和大的表面积,这种特性使得骨架可包封/锚定合适的金属阳离子来获得接枝的原位分离催化剂。此外,这些底物中含有大量具有孤对电子的杂原子(例如,N、S和O),这些杂原子可以作为活性配位点来锚定单个金属原子。通过热解策略获得的单原子材料通常表现出优异的稳定性和相对较高的负载量。目前,已有大量报道关于寻找合适前驱体并开发获得高质量SACs的工作。SACs的高温热解合成主要分为两种:自下而上和自上而下的方法。
自下而上的热解方法中,通过掺杂、吸附或取代可将目标单原子结合到前驱体中。石墨烯、碳纳米管和一些聚合物可以作为单原子合成的前驱体。通过与官能团的静电相互作用和与缺陷的强配位相互作用,目标金属原子可以被吸引并稳定在石墨烯和碳纳米管前驱体表面上。此外,为了提高单原子的负载量,引入杂原子(N、S和O)作为活性位点来锚定目标金属。与含氮前驱体混合并在NH3气氛中热解是增加石墨烯和其他碳材料中N数量的最常用策略。以氧化石墨烯(GO)为载体前驱体,通过Ru与表面含氧基团的静电相互作用稳定Ru(NH3)6Cl3,制备了分散在氮掺杂石墨烯上的Ru-N-C单原子催化剂。然后,Ru-GO前体通过加入Ar和NH3在不同温度下热解以获得均匀分散在N掺杂石墨烯上的孤立Ru原子。
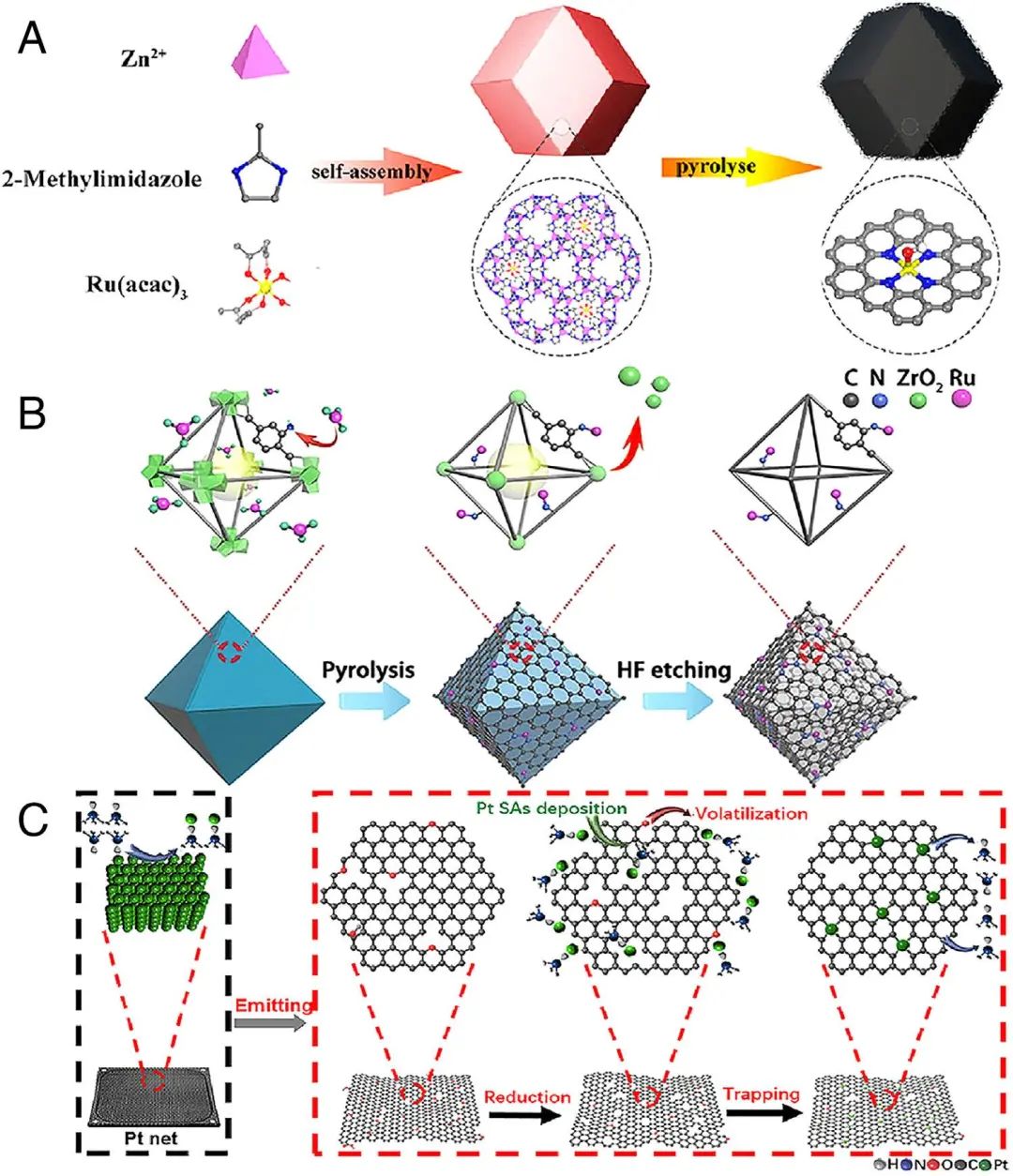
Figure1. Schematic illustration of host−guest strategy for the fabrication of SACs with ZIF-8 as precursor. (B) Schematic illustration for fabrication of SACs anchored by free functional groups. (C) Proposed reaction mechanism for the preparation of Pt SAs/DG via thermal emitting method.
具有高度规则孔径和原子尺度分散金属节点的MOF也可被用作前驱体,然后通过热解策略可制备目标单原子的PMSACs。除了金属载体与配位原子(N、S 和 O)的相互作用外,目标单原子还可以通过MOF丰富的空腔中来稳定。热解过程后,配位分子衍生的碳载体可以提供稳定的骨架,配位原子可以作为锚定活性单原子的活性位点。同时,金属节点确保目标单原子原子水平的分散在碳载体上,同时避免它们在高温下聚集成簇和粒子。腔直径为 11.6 Å的ZIF-8是最常用的前驱体,它可以作为宿主来容纳具有合适直径的各种金属前驱体。此外,ZIF-8的主要金属元素是沸点为905 °C的Zn,Zn可以在高温热解过程中简单去除。通过在ZIF-8前驱体的分子笼中原位封装Ru(acac)3的热解可制备Ru原子催化剂。在热解过程中,Ru(acac)3被转化为原子水平分散的Ru-C/N并均匀锚定在N掺杂的碳骨架表面。此外,在酸中进行预漂白处理可彻底去除SACs中的杂质。如图1A所示,通过在950 °C下热解Ru(acac)3-ZIF-8前驱体合成了分散在N掺杂碳载体上的Ru-NC单点,然后在HNO3中预漂白以去除不稳定物质。在没有Ru-Ru或Ru-O配位结构的情况下,所得的Ru单原子中心催化剂显示出具有吸附OH作用的RuN4纯配位结构。此外,贵金属原子也可以通过金属原子与MOF中的自由官能团之间的强相互作用来锚定(图1B)。Ru3+通过与UiO-66-NH2骨架上的游离胺基 (-NH2) 配位而稳定,并转化为固定在碳骨架上的Ru-NC位点。
自上而下的方法是使用块状金属作为前驱从纳米粒子或热发射中去除多余的原子来合成SACs。热解过程通常辅以腐蚀性气氛例如NH3和PH3,被用来促进颗粒或块状金属中金属键的断裂。利用这种巧妙的策略,前驱体的选择更多、操作也更容易,还可以有效避免前驱体合成过程中贵金属聚集的缺点。例如,PH3辅助催化可以用于在低温(400 °C)下将 Pd 颗粒有效转化为g-C3N4纳米片上稳定的P配位单原子(PdP-SA/CN)。通过PH3与贵金属之间的强路易斯酸碱相互作用对Pd/CN纳米颗粒前驱体进行两次磷化处理制备PdP-SA/CN 催化剂。此外,目标单金属原子也可以从其他块状金属转化为载体。与具有高毒性和易燃性的PH3相比,NH3也可被选为“载气”来合成单原子催化剂。如图1C所示,通过热辐射法合成原子水平分散的Pt。在高温下,原位生成的NH3可以通过强相互作用与Pt配位形成挥发性Pt(NH3)x,随后锚定在有缺陷的石墨烯表面。
高温热解策略具有良好的灵活性、广泛的可选择前体和高产量的特点,是制备SACs最常用的方法。然而,单金属原子中心配位结构的均匀性和高热解温度下纳米粒子的合成过程需要进一步具体控制。
1.2 电催化
电化学沉积是一种改变表面特性或将新成分沉积到材料上的简单而通用的方法来。该方法具有制备简单、控制容易、能耗低、对环境友好的优点。从合成机理来看,SACs的合成主要有两种电化学方法,包括常规电沉积和电位循环法。
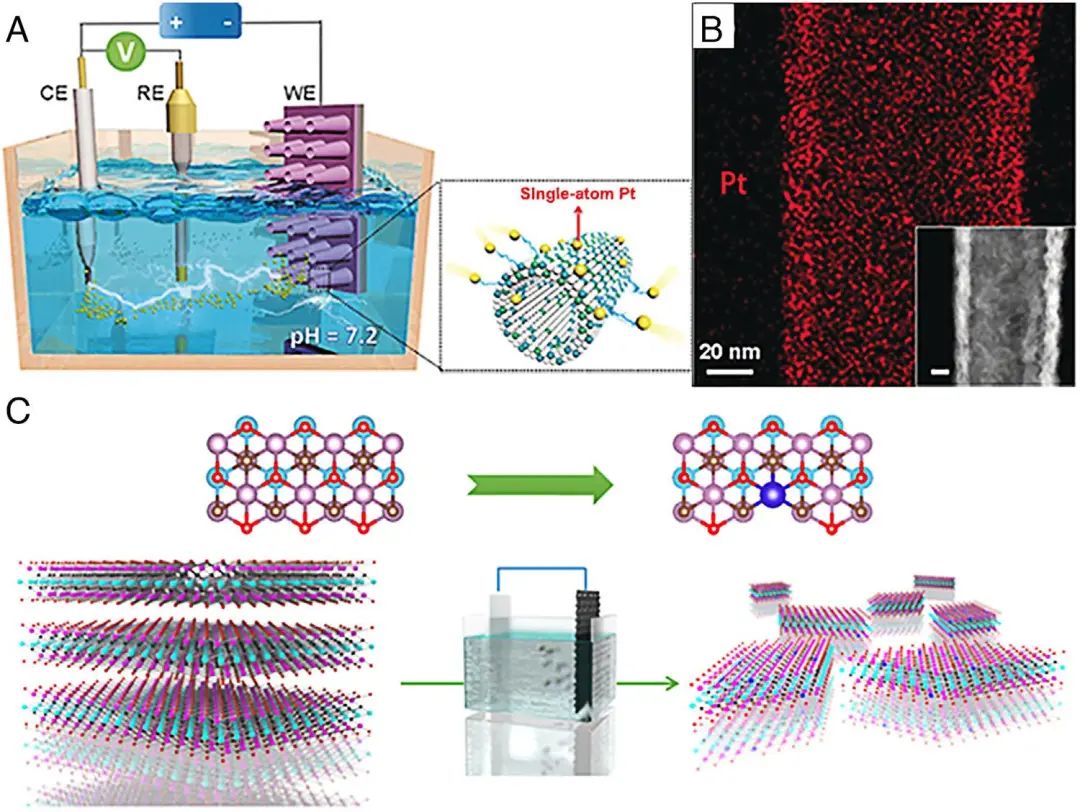
Figure 2. (A) Schematic diagram of the synthesis process. CE represents for counter electrode, which is Pt foil; RE represents for reference electrode, and WE represents for working electrode. (B) EDS map of Pt in a CoP nanotube. (C) Schematic diagram of the electrochemical exfoliation process of MXene with the immobilized single Pt atoms.
对于电位循环法,目标金属原子通常作为辅助电极,在循环过程中可以从阳极溶解到高电位的电解质中并重新沉积到基板(工作电极)上。在这种方法中,铂箔或金属丝是最常用的用于在材料上沉积单个原子的辅助电极。如图2A所示,通过电位循环法,合成了在泡沫镍上生长的CoP纳米管上负载的 Pt 单原子。Pt 原子以相对较高的密度均匀分散在整个CoP纳米管(图2B和C)。此外,载体中的缺陷可以为锚定单个原子提供更多位点,从而提高负载密度和稳定性。如图2D所示,在电化学剥离过程中,MXene上Mo空位形成,单个Pt原子与周围的C原子形成共价Pt-C键同时被固定。
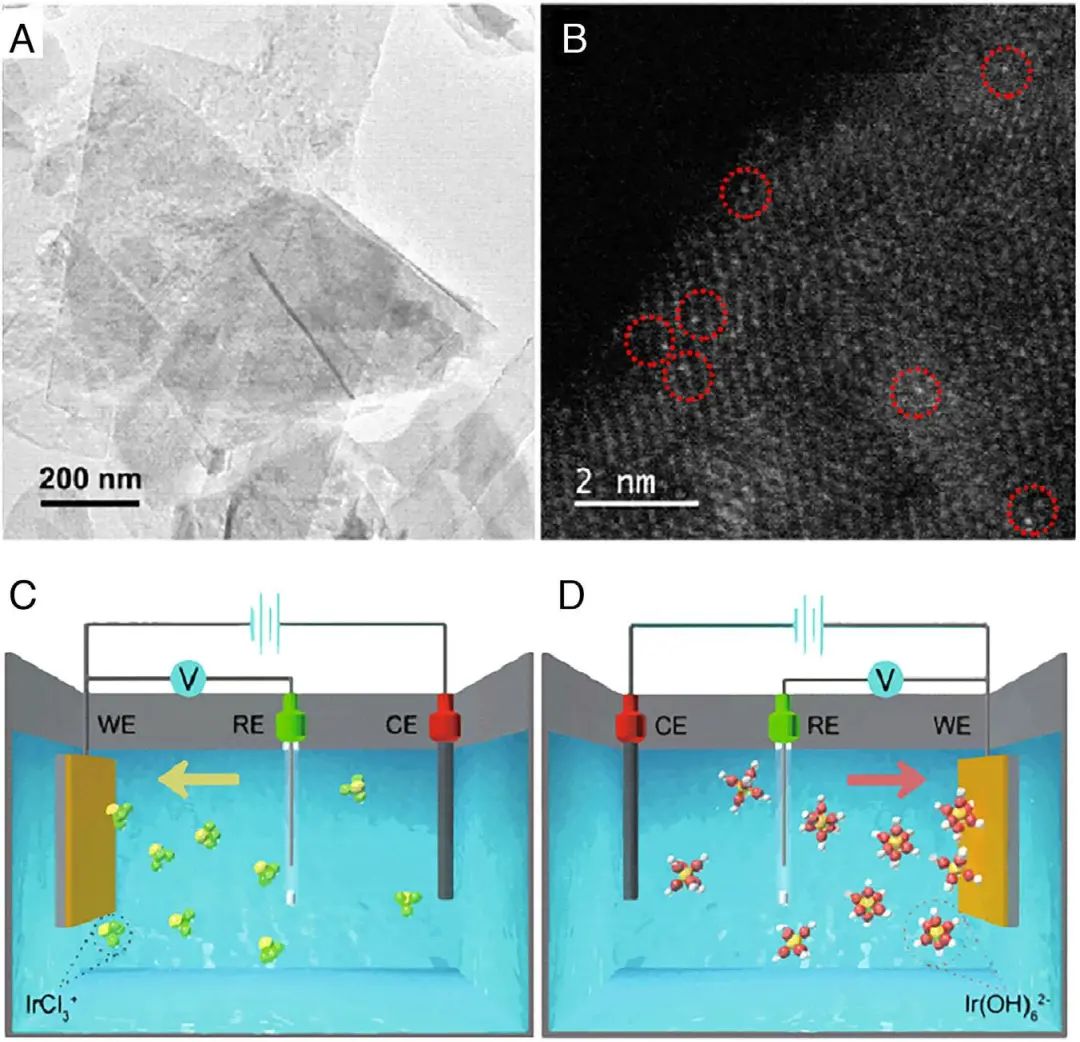
Figure 3. (A) TEM, (B) HAADF-STEM images of sAu-NiFe-LDH. diagram of (C) cathodic and (D) anodic deposition of Ir species. The yellow, green, red, and white spheres represent Ir, Cl, O, and H atoms, respectively.
对于传统的电沉积,目标金属原子预先分散在电解质中,然后被还原到基板(工作电极)表面。与电位循环法相比,传统的电沉积方法可以将更多种类的贵金属掺入载体中。如图3A和B所示,利用HAuCl4作为金属前驱体可制备NiFe-LDH纳米板上负载的单Au原子PMSACs。Au原子以原子态均匀分散在 NiFe-LDH 表面而不是簇或纳米颗粒,表明成功制备了单原子sAu-NiFe-LDH催化剂。该方法可以扩展到各种贵金属和载体中,如Ir、Ru、Rh、Pt、Pd以及氧化物、硫化物、硒化物、碳等。除此之外,SACs还可以通过阴极和阳极沉积合成,对应的SACs分别对HER和OER表现出高活性。通过阴极和阳极沉积过程可合成沉积在Co(OH)2纳米片上的Ir单原子。对于阴极沉积,IrCl3+阳离子被施加的电场驱向阴极,沉积在载体上并与三个O原子配位在Co(OH)2上。随后Ir离子在负电场下被还原,导致Ir单原子氧化态低于+4(图3C)。对于阳极沉积,Ir(OH)6-2阴离子作为沉积物,在电场的驱动下在阳极被氧化,导致Ir单原子的氧化态高于+4(图3D)。
1.3 光化学还原
通过光照射可合成贵金属纳米晶体。光化学还原合成过程包括前驱体的成核和生长,最后转化为金属纳米晶体。这一过程中,为了生成均匀分散的金属单原子,应尽可能降低成核反应速率。通过使用紫外(UV)光对冷冻氯铂酸溶液进行光化学还原,可制备原子水平分散的Pt催化剂。其中,低温光化学还原反应防止了原子的聚集,成功稳定了单个原子。随后,将水替换成乙醇和水的混合物并在超低温(-60°C)下进行光化学还原,显着提高了反应动力学势垒并抑制了金属原子的成核。此外,贵金属原子也可以锚定在各种固体载体上。Pd单原子在冻结状态下可通过原位光化学还原固定在TiO2上。辐照激发TiO2产生电子,随后促进PdCl42-还原并形成固定在TiO2上的单个Pd原子。此外,具有高度不对称电子分布的原子配位Pt-Co-Se可以通过缺陷(Se空位)锚定和并且通过光化学还原来稳定Pt单原子到CoSe2表面上来合成SACs,所得催化剂具有较高的Pt负载量和优异的OER性能。
光化学还原策略具有环保、低能耗、高效、易操作等特点。然而,由于溶剂是水,在0°C很容易冻结,导致这种策略不适用于在水溶液中不稳定的载体。此外,为了产生强金属-载体相互作用,载体需要具有光响应性或具有丰富的缺陷或杂原子。并且,除Pt和Pd外,一些贵重金属原子对辐照反应不灵敏,因此光还原效果并不是很理想,导致载体种类和单金属原子的选择相对有限。
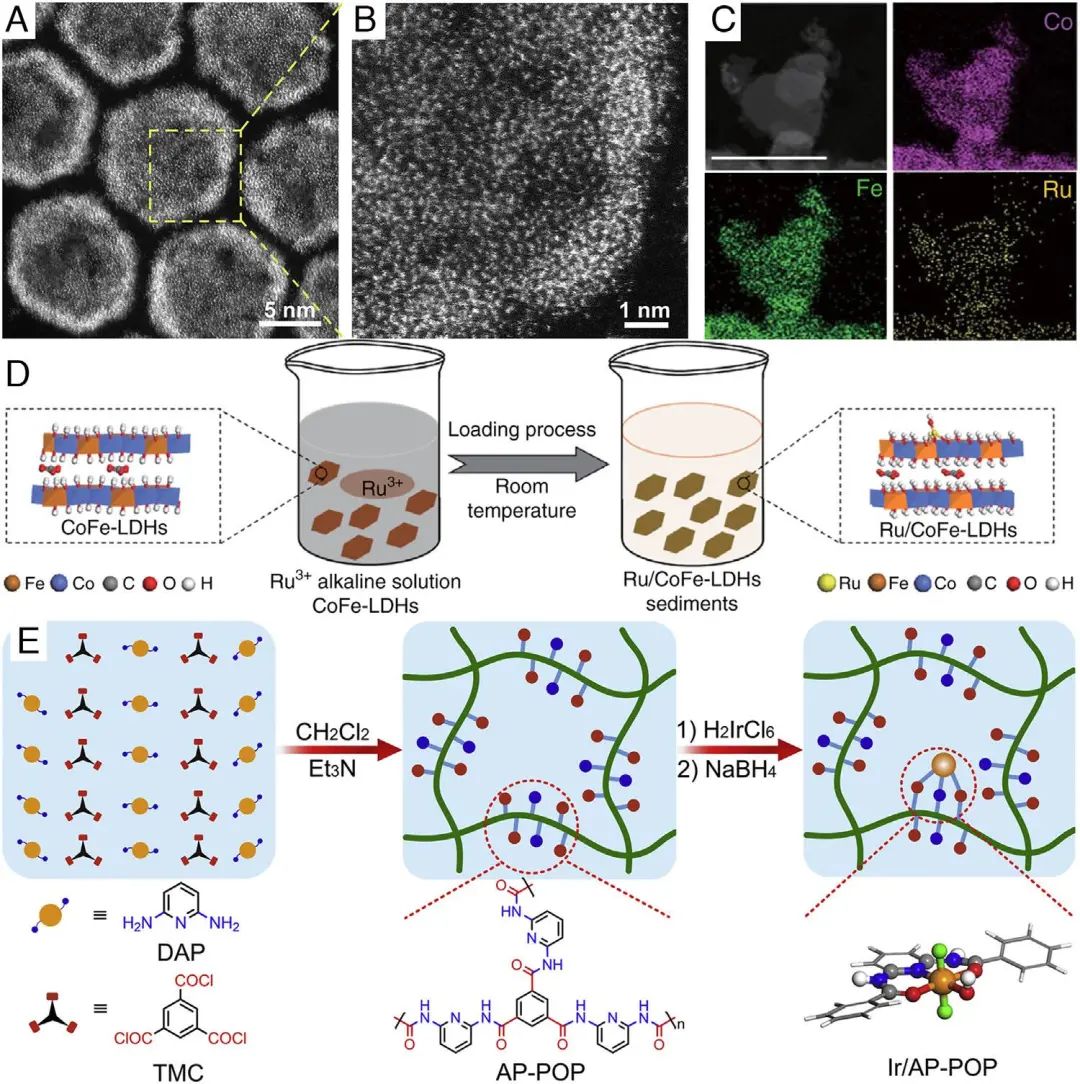
Figure 4. (A, B) HAADF-STEM images of h-Pt1-CuSx. C) The HAADF-STEM images and elemental distribution of Ni, Fe, and Ru in the Ru/CoFe-LDHs. Scale bar, 50 nm. (D) Schematic illustration of the impregnation method to form Ru/CoFe-LDHs. (E) The schematic illustration of the synthesis of Ir/AP-POP SACs via chemical reduction method.
基于金属离子不同迁移率的离子交换法,可用来合成高负载量的孤立金属原子催化剂。如图4A和B所示,通过离子交换方法合成了嵌入中空无定形CuSx载体(h-Pt1-CuSx)中原子水平分散的Pt PMSACs,同时实现了极高的Pt负载量 (24.8 at%)。Pt与载体之间的相互作用是构建高负载量和稳定的单原子分散催化剂的关键,Pt-S键的亲和力强于Pt-N和Pt-O。此外,利用浸渍法可以在温和的条件下合成SACs。如图4C和D所示,Ru单原子在室温下通过浸渍法均匀地结合到CoFe-LDHs中。金属前驱体(RuCl3)被充分水解形成羟基配合物,并通过脱水反应固定在CoFe-LDHs表面。共沉淀法操作简单,产量高,是制备纳米材料的常用方法。在NaBH4的协助下,通过快速合成制备了单个Ir原子锚定的ɑ-Co(OH)2。Ir与ɑ-Co(OH)2通过Ir -Co配位相互作用稳定孤立的Ir原子。化学还原是另一种广泛采用的合成簇和纳米粒子的方法,通过控制金属前驱体的添加量、反应温度和时间可控制合成SACs。图4E描述了通过温和的水热还原过程合成修饰在多孔有机聚合物 (AP-POP) 上的Ir单原子。H2IrCl6前驱体首先被AP-POP中的阴离子基团捕获,然后还原为N、O配位的Ir单原子。
湿化学方法是一种可被用于构建具有广泛选择的金属原子和载体种类的 SACs传统但有效的方法。此外,应注意避免在反应过程中形成簇和纳米颗粒。到目前为止,湿化学方法是生产用于商业应用的SACs的最有前景的策略。
1.5 其它方法
原子层沉积 (ALD)是一种将薄膜沉积到基板上的气相沉积方法。ALD过程大致包括金属前驱体蒸汽交替脉冲进入反应物室并化学吸附在基板上。ALD方法可以应用于SACs的合成,并且可以通过调整ALD循环次数来精确控制单原子的数量。这一过程中,因为前驱体无法避免的在 ALD 工艺中化学吸附到载体上,所以选择合适的前驱体对于沉积原子至关重要。如图5A所示,通过 ALD 方法合成了负载在N掺杂石墨烯纳米片上的孤立的单个铂原子和簇。Pt前驱体 (MeCpPtMe3)首先与N掺杂石墨烯中的N掺杂位点反应,然后在暴露于O2时完全氧化为CO2和H2O,从而形成含Pt的单层。值得注意的是,在沉积的Pt表面形成了一层新的吸附氧,这为下一个ALD循环过程提供了官能团。此外,液体激光烧蚀 (LAL)具有很强的淬火效应,可被用于制备具有亚稳态纳米结构的材料。使用纳秒激光制备的Ru纳米颗粒上单独放置Au原子的单原子合金(SAA)(脉冲宽度为7 ns)照射Ru靶(图5B),导致固体靶的蒸发、HAuCl4的热分解以及随后在快速淬火过程中RuAu SAA的形成。ALD和LAL技术可以快速合成单一的贵金属原子催化剂,为探索金属-载体相互作用和结构-性能关系提供了极好的模型。然而,由于成本高、产量低,这些技术可能不适合商业应用。
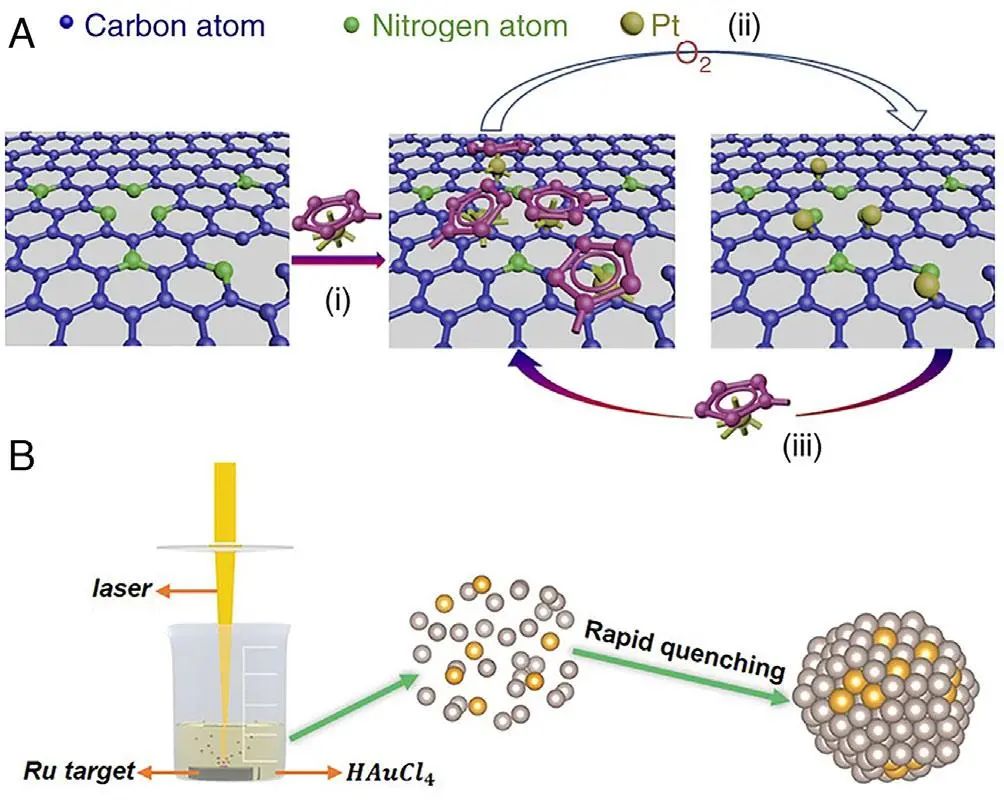
FIigure 5. (A) Schematic illustration of the Pt ALD mechanism on NGNs. (B) The schematic setup of LAL and the formation process of SAA nanoparticles.
2. SACs的表征
表征技术在深入理解原子结构和开发大量具有新结构的PMSACs方面发挥着重要作用。随着先进表征技术的发展,使用扫描透射电子显微镜(STEM)可以直接观察原子水平上单个金属位点的精细结构。分辨率低至亚埃的像差校正STEM (AC-STEM)可以清楚地区分单个金属原子与不同亮度的载体。一般来说,随着孤立原子和载体之间的原子序数差异越大,原子金属斑点的明显程度越明显。此外,电子能量损失谱(EELS)与AC-STEM结合可用于分析单个原子位点周围的元素组成。
与主要关注SACs局部区域中孤立原子的电子显微镜相比,同步加速器X射线吸收光谱(XAS)通常用于研究单个原子位点的整体和平均结构。相应的X射线吸收精细结构(XAFS)可以揭示孤立活性位点的电子结构和配位环境,这对于确认和分析SACs的具体结构是必不可少的。傅里叶变换扩展X射线吸收精细结构(FT-EXAFS)得到的径向结构函数(R空间)可以根据活性金属之间的径向距离检测背向散射路径,直观地将孤立的原子位点与团簇和粒子区分开来。结果,归因于金属-非金属原子(N、C、O、B、P 等)的配位,孤立的原子位点催化剂只显示一个主峰,不存在同时分配给团簇或粒子的金属-金属配位(在~ 2 Å)。此外,根据实验EXAFS数据,可以通过最小二乘曲线拟合模拟在短距离内与单个原子位点配位的原子的配位数、种类和距离。因此,AC-STEM和XAS的结合可以成为研究孤立原子周围精细结构信息的有效策略,已成为分析SAC的原子色散、配位环境和电子结构的标准测量方法。
3. 用于水分解催化的贵金属单原子材料
大量的PMSACs已被用于催化电化学水分解反应 (2H2O → 2H2 + O2)。如上所述,SACs具有最大的原子利用率、明确的活性位点和独特的电子结构,因此可以表现出优异的催化性能,并可为探索反应机理提供理想模型。
3.1 HER
析氢是通过电化学水分解方法制氢的核心反应。HER是一种双电子转移过程,其可以在很宽的pH值包括酸性 (H2SO4)、中性 (PBS) 和碱性 (KOH) 电解质中进行。正如引言中提到的,HER有两个过程:Volmer-Heyrovsky和Volmer-Tafel过程。HER催化主要包括质子或H2O分子的适当吸附、质子的快速结合以及反应过程中电子快速进入活性位点,这些是提高HER表现的主要方面。
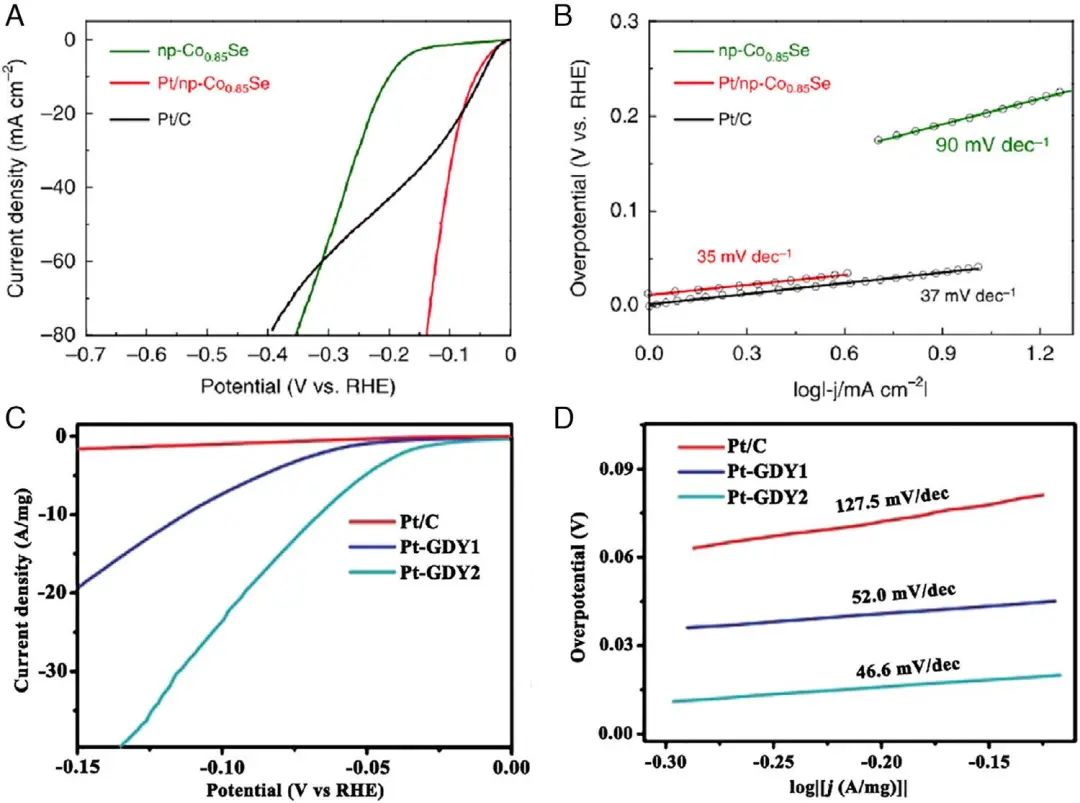
Figure 7. (A) HER polarization curves and (B) corresponding Tafel plots of np-Co0.85Se, Pt/np-Co0.85Se, and Pt/C. (C) The polarization curves and (D) corresponding Tafel plots for Pt-GDY1, Pt-GDY2, and commercial Pt/C in 0.5 M H2SO4.
对于Pt基SACs,单原子Pt被广泛认为是真正的活性中心。Pt基SACs在HER过程中的反应机制在很大程度上取决于载体的种类和制备方法。遵循 Volmer-Tafel过程,通过电化学电位循环法合成的Pt基SACs通常表现出相对较低的塔菲尔斜率。例如,通过电化学方法制备的3D纳米孔Co0.85Se负载单Pt原子催化剂在10 mA/cm2下显示出55 mV的过电位和35 mV/dec的塔菲尔斜率(图7A和B)。为了增加单原子的负载密度,具有更大比表面积的电极被用作目标贵金属原子的载体。通过电位循环法制备了Pt单原子锚定的CoP纳米管无粘合剂电极,在10 mA/cm2时显示出24 mV的过电位和30 mV/dec.的塔菲尔斜率。可以推断出这种Pt-SACs的Volmer-Tafel机制载体可以在制备过程中被激活,从而增加活性位点的有效暴露,导致表面吸附的H快速结合。此外,在3D 无粘合剂载体上装饰的单原子可以增强电子传输,从而改善反应动力学。Volmer-Heyrovsky过程也在基于Pt的SACs中被发现用于HER时,其载体通常具有相对较差的 HER 性能。如图7D和E所示,通过湿化学方法修饰在石墨二炔上的Pt单原子在-0.1V下显示出23.64 A/mg的电流密度和46.6 mV/dec 的塔菲尔斜率,优于商业Pt/C电极。
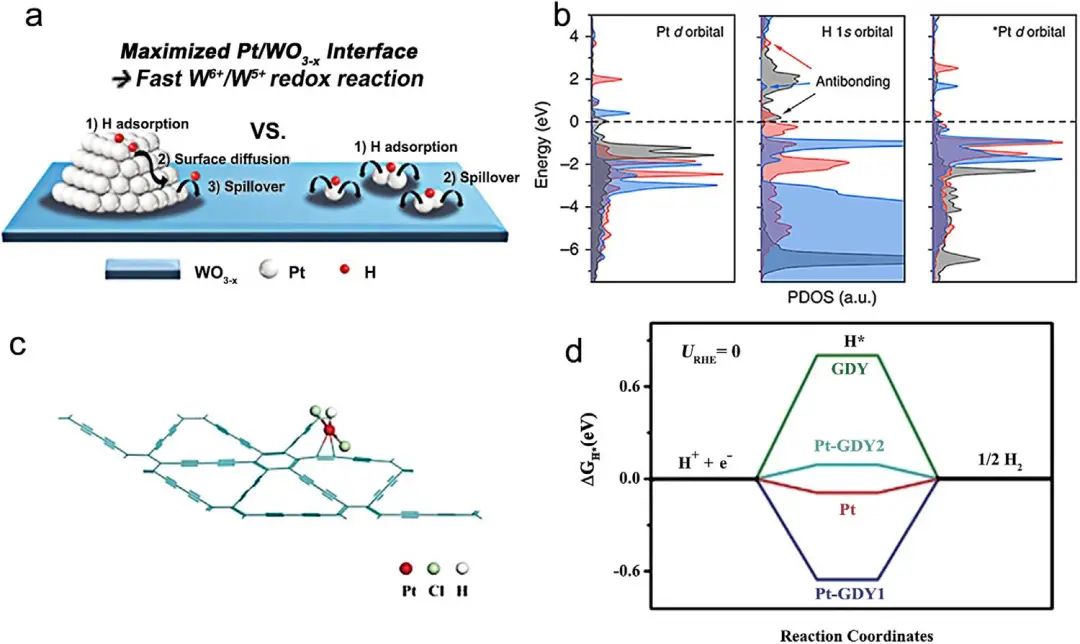
Figure 8. (A) Illustration of the HER for single atom and nanoparticle Pt/m-WO3-x. (B) Calculated PDOS of Pt d orbital of clean surfaces. (C) The configuration of Pt-GDY2 with hydrogen adsorbed on. (D) The calculated Gibbs free energy diagram for hydrogen evolution on different catalysts.
此外,在单原子Pt/m-WO3-x催化剂上提出了一种新的氢溢出效应机理。在单原子Pt/m-WO3-x中,Pt和氧化钨之间的最大界面减少了氢扩散长度,因此导致了更快的氢插入/提取动力学和增强的氢溢出效应(图8A)。加速的氢插入/脱出可以诱导Pt表面的快速重新暴露并允许另一个H+的吸附,从而加速HER过程。一般来说,与粒子和块体对应物相比,源自载体金属的强相互作用,基于Pt的SACs显示出独特的电子结构。Pt的5d轨道的PDOS显示出接近费米能级的高电子密度,与纯载体相比,这可以促进H+吸收并提高电导率(图8B)。此外,基于Pt的单原子电催化剂的中间态 (ΔGH) 的吉布斯自由能更接近于零,这意味着与本体Pt对应物相比,基于Pt的SACs具有更高的固有HER活性(图8C和D)。Pt单原子独特的电子结构和高原子利用率导致Pt基SACs具有优异的比质量活性。
除了基于Pt的SACs,科学家们还开发了基于Ru-和Rh-的PMSACs。利用 Ru 装饰MoS2,合成了性能优异的SACs,并将其应用于碱性HER。Ru原子引入MoS2后,从2H到1T的相变和S空位的产生降低了Volmer过程的能垒和H *的吸附/解吸,同时提高了电导率。此外,分散在Mxene上的N、S配位的Ru单原子在10 mA/cm2下显示出76 mV的过电位和90 mV/dec的塔菲尔斜率。此外,Rh 原子可被嵌入MoS2中并在0.5 M H2SO4中对HER表现出优异的活性。Rh原子取代了Mo原子,并按照一定距离分散在晶格中。同时,可以通过改变受限的Rh原子的距离来调节与Rh原子相邻的面内S位点的HER活性,从而激活MoS2中的惰性平面,提高 HER 性能。HER也采用了一些SAA催化剂。采用新型RuAuSAA作为碱性HER的催化剂,RuAuSAA在10 mA/cm2下表现出 24 mV的低过电位和 37 mV/dec的低塔菲尔斜率。
3.2 OER
由于OER过程中的四电子转移动力学过于缓慢,导致了水氧化是降低电化学水分解制氢过程中过电位和能耗的关键反应。因此,迫切需要具有优异活性和稳定性的电催化剂来克服这些问题。为了有效提高OER的内在催化活性,活性中心的电子结构需要通过单个贵金属原子和载体之间的相互作用进行调控。有两种策略可以提高SACs的OER性能:合并新的活性位点并同时增强原始活性位点的活性。
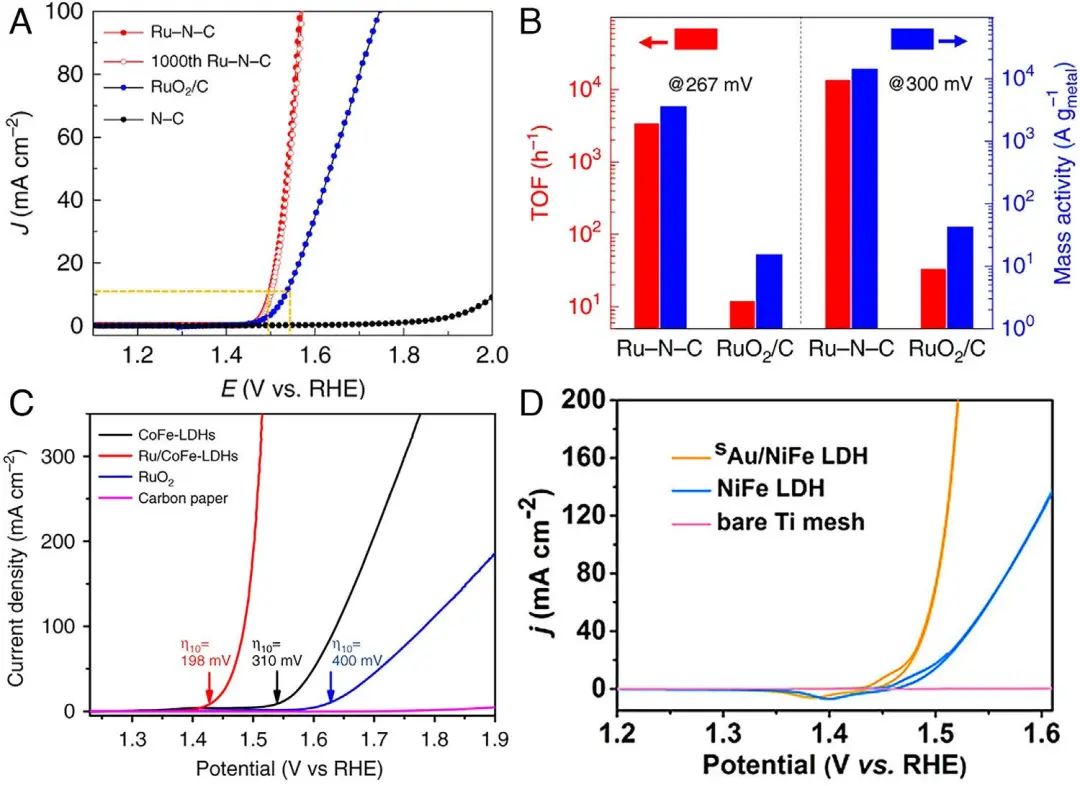
Figure 9. (A) Electrocatalytic OER LSV and (B) TOF and mass activities of Ru-N-C in 0.5 M H2SO4. (C) OER polarization curves of Ru/CoFe-LDHs and CoFe-LDHs. (D) Cyclic voltammetry curves for sAu/NiFe-LDH and pure NiFe-LDH in 1 M KOH.
当锚定在具有OER活性的载体上时,新引入的单原子也可以成为活性中心。如图9A和B所示,将单原子分散的Ru-NC电催化剂应用于酸性OER中,在10 mA/cm2下表现出267 mV的低过电位和在300 mV下的高TOF(13 392O2/h)。由于(杂原子掺杂)碳载体在基于金属-NC的SACs中的OER活性基本上可以忽略不计,因此水氧化的活性中心通常被认为是孤立的金属原子。此外,可采用具有良好OER活性的材料作为载体来锚定单个贵金属原子,以提高 PMSACs的OER活性。如图9C所示,合成了CoFe-LDH负载的Ru基SACs,在10 mA/cm2下显示出 198 mV 的低过电位。这其中,OER性能的增强主要归因于单原子Ru和LDHs之间的强协同电子耦合。除此之外,制备了具有高负载量(18 wt% Ir)的Ir修饰的NiO纳米片电极,在10 mA/cm2的碱性OER下显示出215 mV的低过电位,而这里增强的原因是由于高负载密度和由原子分散的Ir引起的Ir-O 键的形成。一些贵金属原子被原子尺度的引入到本身具有优异OER活性的载体中,例如 NiFe-LDH,可以通过调整原始活性位点的电子结构来提高OER活性。如图9D所示,NiFe-LDH电极上负载的Au单原子在10 mA/cm2下对于碱性 OER 显示出280 mV的低过电位。Au原子的掺入可以诱导由Au到LDH电荷重新分布,从而转移到周围的O、Ni和Fe原子。这种特定的电子结构可以促进OH−的吸附并改变O* 和OOH*中间体的吸附能,从而提高OER性能。此外,这两种方法都可以增强PMSACs的OER活性。将Ir单原子固定在Co纳米片上的电催化剂在1 M KOH中以10 mA/cm2显示出267 mV的低过电位。Ir-Co 双核位点是新的活性中心,其中羟基倾向于吸附在Co位点上并解离成吸附的O*,然后通过 Co-O-Ir中间体进一步转移到Ir-O*。
PMSACs的稳定性可以通过单原子金属-载体相互作用设计电子结构来改善。RuO2是商业 OER 应用较为广泛的催化剂。然而,由高氧化状态的Run+解离到电解质中导致OER 稳定性差。用 Ru 单原子电催化剂修饰的 Pt-Cu 合金证明了Pt的压缩应变可增强RuO2稳定性。Pt-Cu 合金可以作为电子储存器向反应中间体提供电子,从而抑制Ru单原子的过氧化和溶解。除此之外,氢氧化物中的非金属元素也可以通过金属-载体相互作用锚定在CoFe-LDH上从而稳定Ru原子。在OER过程中,Ru/CoFe-LDH中Ru的氧化态低于+4,因此可以抑制Ru离解,提高稳定性。
此外,PMSACs也可以应用为面向OER和HER的双功能电催化剂。已报道的研究工作表明,基于Ir的SACs是在酸性和碱性介质中双功能催化水分解的有望候选者。通过Ir-ZIF-67前驱体的热解,Ir单原子分散在N掺杂的碳和Co颗粒上,在1.0 M KOH电解液中只需1.603 V的电位即可达到10 mA/cm2。当结构材料被用作载体时,PMSACs的催化水分解活性可以大大提高。利用电化学沉积在镍泡沫上生长的Co0.8Fe0.2Se2纳米片上修饰了Ir单原子,在碱性电解质中仅需 1.39 V的电压即可达到10 mA/cm2。
4. 总结与展望
最后,对开发适用于电化学水分解应用的新型贵金属单原子催化剂所面临的主要挑战和机遇进行了总结与展望。电催化水分解是一种可以减少环境污染问题和提高能量转换效率有效的制氢方法。开发高效的OER/HER催化剂是电化学水分解实际应用的关键。将贵金属催化剂缩小为单原子态不仅可以大大提高原子利用率,而且由于单金属原子与载体之间的强相互作用,还可以提高内在催化活性。目前,已经开发了较多的方法被用来合成高质量的PMSACs,包括高温热解法、电化学法、湿化学法、光化学法和其他新方法。通过AC-STEM结果可以清楚地观察到PMSAC中单个原子位点的特定结构和分散状态。此外XAFS通常用于排除簇或粒子的存在,并确认单个原子位点周围的配位状态。因此,归因于通过掺入单个原子在活性中心进行的电子结构变化,PMSACs在各种pH溶液下的水分解中对OER和HER均表现出优异的活性和稳定性。
尽管已经致力于开发具有高性能的水分解PMSACs,但仍有一些问题需要解决和进一步改进。
1.为了获得高比质量/面积活性催化剂以提供丰富的电催化活性中心,需要进一步提高 SACs中有效暴露的单原子位点的负载密度。增加的单原子位点可以满足与吸附的H结合以产生高H覆盖率的H2分子的要求,从而促进HER过程。目前,SACs中贵金属的负载量相对较低(大多<10 wt%),仍有很大的改进空间。此外,选择具有高比表面积和锚定位点(缺陷、杂原子、悬挂键等)的合适载体对于提高SAC中的单原子密度也至关重要。
2.原子水平活性位点的结构研究对于理解反应机理和构效关系非常重要。到目前为止,最有效的表征技术包括AC-STEM和EXAFS。此外,理论计算和运算元表征也可被用来为电催化过程中某些特定点的结构和能量变化提供一些基础信息。然而,在电化学水分解过程中,从空间和电子方面原位检测单个原子位点的结构演变和吸附中间体的变化仍然很困难。因此,仍然需要新的表征技术来为催化过程中单个原子位点的实时变化提供直接而详尽的信息,这对推断PMSACs的反应机理和揭示其电化学催化水解的构效关系具有指导意义。
3. PMSACs 由于其固有的活性优势,在工业电化学制氢方面极具吸引力。然而,目前的主要挑战在于PMSACs的稳定性较低,尤其是在高单原子金属负载密度下。工业应用中催化剂稳定性的时间尺度通常为数月甚至数年,远长于实验室研究。因此,如何在电催化水分解过程中使活性位点保持原始结构并避免金属原子的聚集或浸出对于后续开发高效稳定的PMSACs起着至关重要的作用。如果这个问题得到有效解决,PMSACs将成为大规模制氢工业化应用的有力候选者。






暂无评论
发表评论