01 文章亮点
1. 在常温常压条件下,将废硝酸盐 (NO3-)电催化还原有价值的氨 (NH3) 是一种绿色环保且有吸引力的,可用于替代 Haber-Bosch 工艺的方案。然而,该反应需要多步电子和质子转移,这使得以节能方式实现高速合成 NH3,成为了一项巨大挑战。
2. 在这项工作中,作者提出了一种串联催化剂的设计概念,该概念涉及耦合不同过渡金属的中间相(存在于低施加的过电势下),作为协同活性位点,使 NO3- 到 NH3的级联转化成为可能。具体而言,作者通过将 Cu-Co 二元硫化物电化学转化为核壳 Cu/CuOx 和 Co/CoO 相来实现这一概念。
3. 电化学测试、动力学研究和原位拉曼光谱表明,内部 Cu/CuOx 相优先催化 NO3-还原为 NO2-,然后,NO2-在附近的 Co/CoO 壳中被迅速还原为 NH3。这种独特的串联催化剂体系可以实现 93.3 ± 2.1% 的 NO3- 到 NH3的法拉第效率, 1.17 mmol cm-2 h-1 的高 NH3产率(@-0.175 V vs. RHE),半电池能效约为 36%,超过了之前的大多数催化剂。
02 前言导读
氨 (NH3) 是肥料和各种化学品的关键原料,也是最有前景的无碳能源载体之一。目前,工业 NH3 合成严重依赖能源和碳排放密集型 Haber-Bosch (H-B) 工艺。最近,使用水作为质子源的电催化 N2 到 NH3 转化 (eN2–NH3),由于其温和的工作条件和低的能量消耗,引起了广泛的研究兴趣。然而,N2的固有特性,包括N≡N键的高解离能(945 kJ mol-1)和低水溶性,使得eN2-NH3的选择性不足,产率比H-B 过程低两个数量级。为了弥补这一差距,对氮循环的了解,重新引起了人们对活性含氮物质(例如 NO 和硝酸盐)向 NH3转化的关注。其中,硝酸根 (NO3-) 阴离子特别具有吸引力,因为它具有较低的 N=O 键解离能 (204 kJ mol-1),并且作为污染物,广泛存在于农业和工业废水中。此外,等离子体技术的初步发展,有望以低能耗将空气转化为 NO3−。因此,使用 NO3−作为前驱体有望实现 NH3 电合成,并为修复环境污染,开辟了一条经济的途径。 微生物中的 NO3- 到 NH3转化是一个串联过程,即,使用硝酸盐还原酶将 NO3- 还原为 NO2-,然后使用亚硝酸盐还原酶或固氮酶将 NO2-转化为 NH3。这种基于酶的串联系统,允许在自然界环境条件下有效地生成 NH3。然而,由于 NO3- 的对称 (D3h)共振结构和与 H2O的强氢键作用,NO3- 通常对水性电解质中的过渡金属表现出低的亲和力。此外,NO3-到NH3途径涉及复杂的八电子转移和多个中间体。因此,过渡金属表面上 NO3-、NO2-和其他含氧中间体(例如 NO)的结合强度之间存在比例关系。优化一种物质的吸附通常会使其他物质偏离其最佳状态,这使得同时加速连续的 NO3- 到 NO2-,和 NO2-到 NH3 反应具有挑战性。 由于铜 (Cu) 基催化剂具有良好的NO3-结合能力,和催化 NO3- 到 NO2-转化的能力,因此,研究人员已针对 NO3-还原反应 (NO3RR) 进行了深入研究。然而,纯铜催化剂通常会因对 NO3RR 中间体(例如 NO2- 和 NO)的强吸附而快速失活。最近,通过调节质子或电子转移,以及吸附在铜中心上的部分还原中间体的结合强度,来突破这些限制。这可以通过将 Cu 与其他过渡金属(例如 Pt、Pd 和 Ni)或金属氧化物(例如 Cu2O)形成杂化物来实现。这些策略已将 NH3 的法拉第效率 (FE) 提高到了70-100%,并将 NH3 产率提高到了 30-200 μmol cm-2 h-1 的水平。然而,这些策略仍需要高的 NO3-浓度(例如,1 M),和/或相对较高的过电位(<-0.4 V vs. RHE)来实现。为了与 H-B 工艺竞争,因此,研究人员非常需要在提高产率和降低能耗方面取得进一步的提升。
03 图文速读
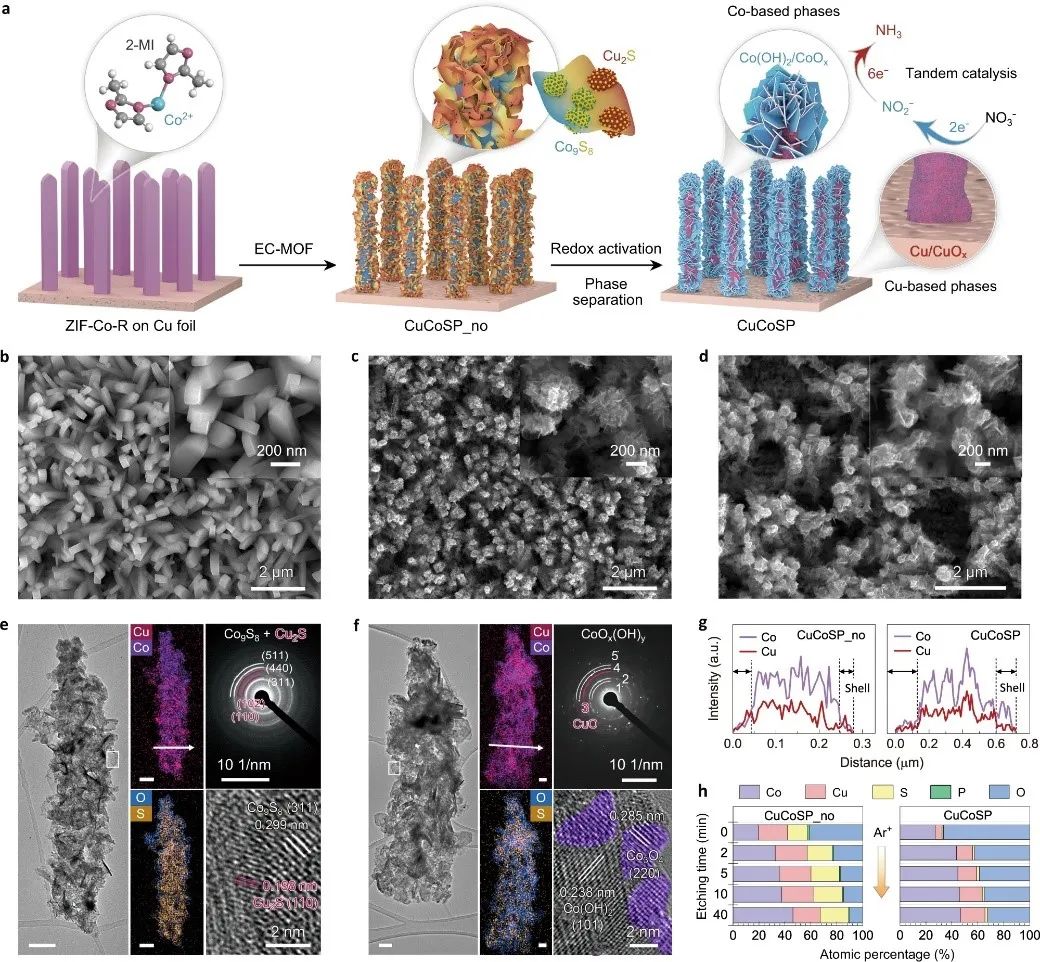
图 1:催化剂的结构表征。a 制备 Cu/Co 基二元“串联催化剂”的示意图。铜箔基板上,ZIF-Co-R 前体 (b)、CuCoSP-no (c) 和 CuCoSP (d) 的 SEM 图像。插图是更高放大倍率的 SEM 图像。e, f CuCoSP-no(e) 和 CuCoSP (f) 的TEM 图像、EDX 元素mapping图、SAED 图案和 HR-TEM 图像。g 由 (e) 和 (f) 中的白色箭头标记的选定区域 EDX 线扫描曲线。h 不同Ar+ 蚀刻时间XPS 确定的 CuCoSP-no和 CuCoSP 的元素原子百分比的深度分布。
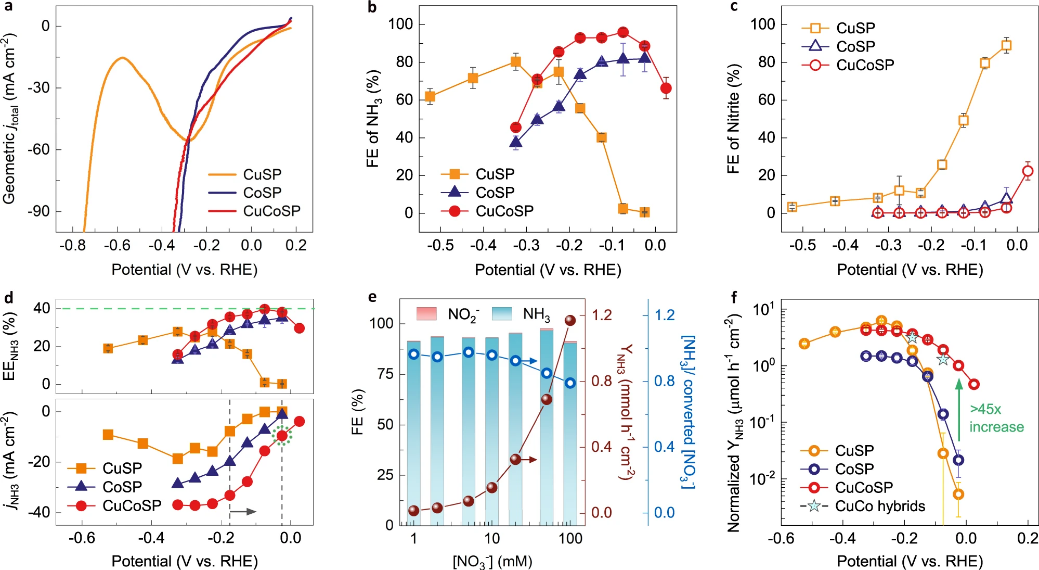
图 2:NO3-到 NH3的转化性能。在含有 0.01 M NO3−的 0.1 M KOH(pH 13) 溶液中,CuSP、CoSP 和 CuCoSP的 (a) LSV曲线,以及在不同电位下的 (b) NH3和 (c) NO2−的法拉第效率 (FE)。d 在不同电位下,CuSP、CoSP 和 CuCoSP 催化剂上,半电池能量效率和 NH3(jNH3) 部分电流密度的比较。e 在 -0.175 V vs RHE时,CuCoSP 催化剂上的NO2-和 NH3的 FE,和NH3产率 (YNH3),以及形成的 NH3浓度 [NH3] 与转化的 NO3-浓度 [NO3-]的比值。f 在含有 0.01 M NO3−的 0.1 M KOH(pH 13) 溶液中,不同催化剂在不同电位下的ECSA 归一化的 YNH3。
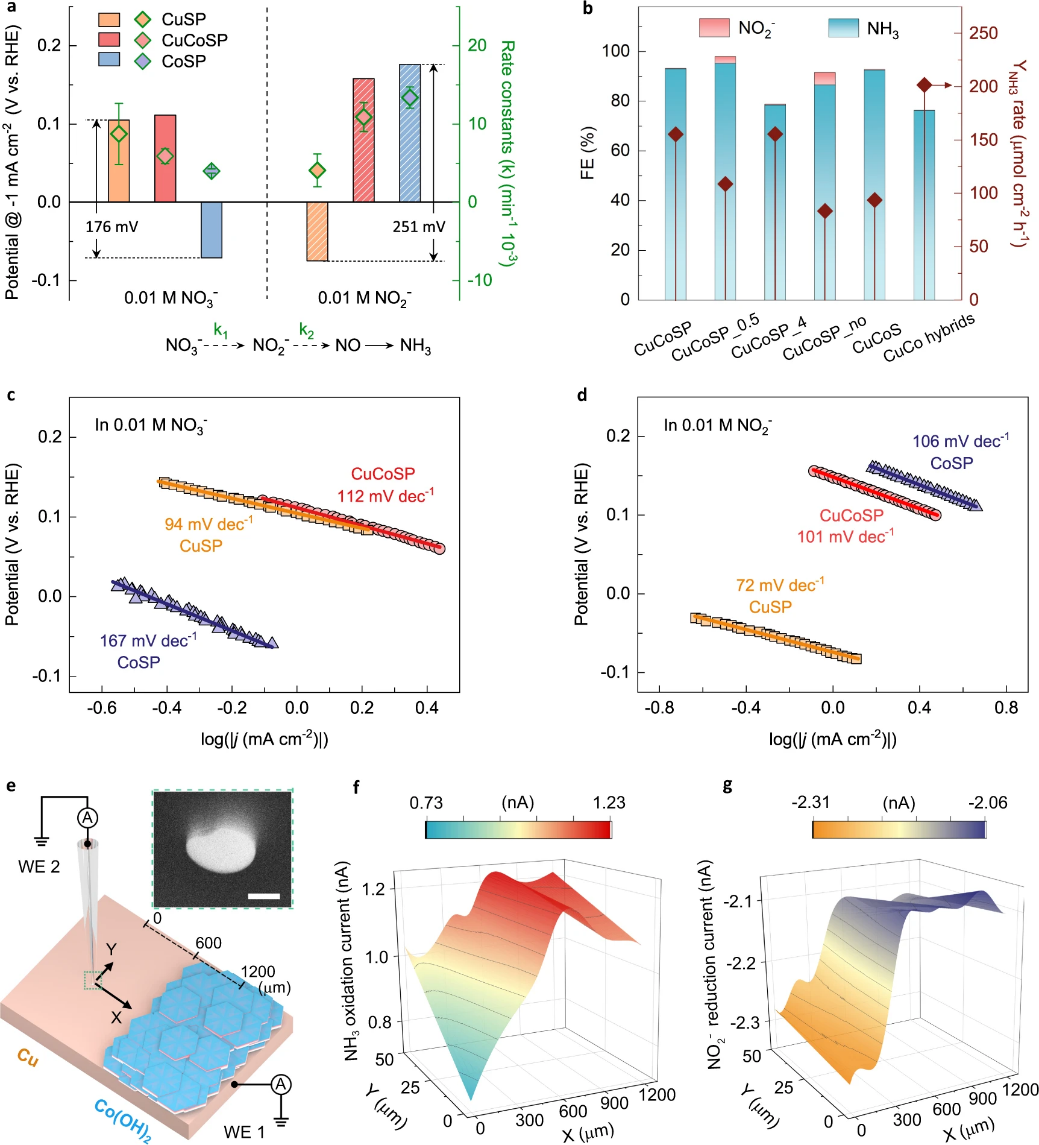
图 3:NO3RR 催化的反应动力学和机理。a CuSP、CoSP 和 CuCoSP 催化剂在电流密度为 -1 mAcm-2时,从 LSV 得到的反应电位和计算的 NO3-和 NO2-还原的反应常数(k,k1 用于 NO3-到 NO2-转换, k2 用于 NO2-到 NO 转换)。b 不同催化剂上的 FE 和 YNH3对比。在 0.01 M 硝酸盐 (c) 和亚硝酸盐 (d) 中,CuSP、CoSP 和 CuCoSP 的Tafel 斜率。e SECM 装置的示意图,该装置在样品生成尖端收集 (SG-TC) 模式下使用 Pt-UME (WE 2) 检测催化剂上 NO3RR 期间产生的 NO2-和 NH3(WE 1)。插图:Pt-UME 尖端的 SEM 图像;比例尺为 500 nm。f, g 当电位为 -0.12 V(vs. RHE)时,在 Pt-UME 上分别记录的 0.76 V 和 0.06 V(vs. RHE)的 NH3氧化(f)和 NO2-还原(g)电流图。
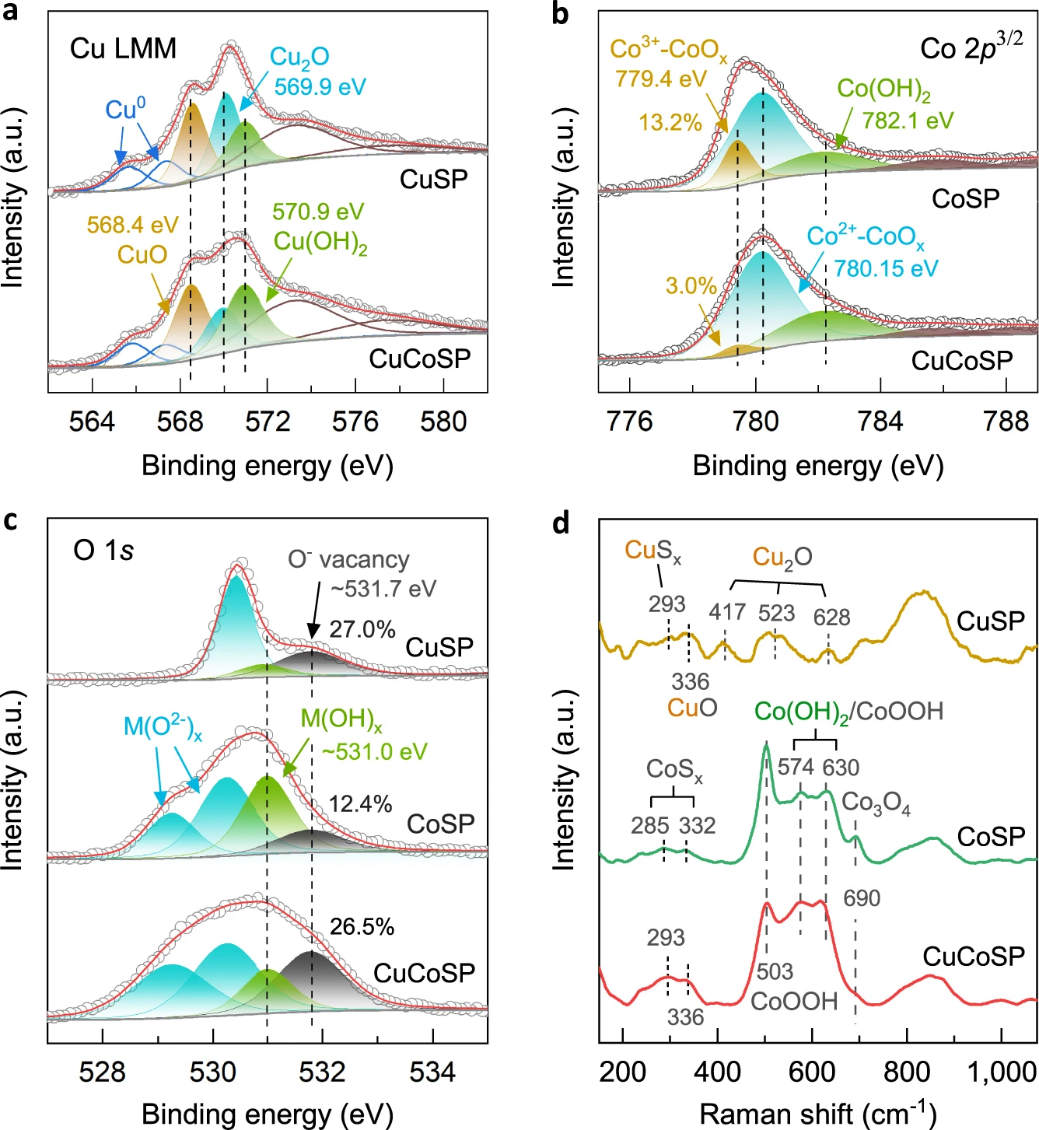
图 4:CuSP、CoSP和CuCoSP催化剂的表面相成分。不同催化剂的 Cu LMM (a)、Co 2p3/2(b) 和 O 1s (c) XPS 光谱。d 非原位拉曼光谱。
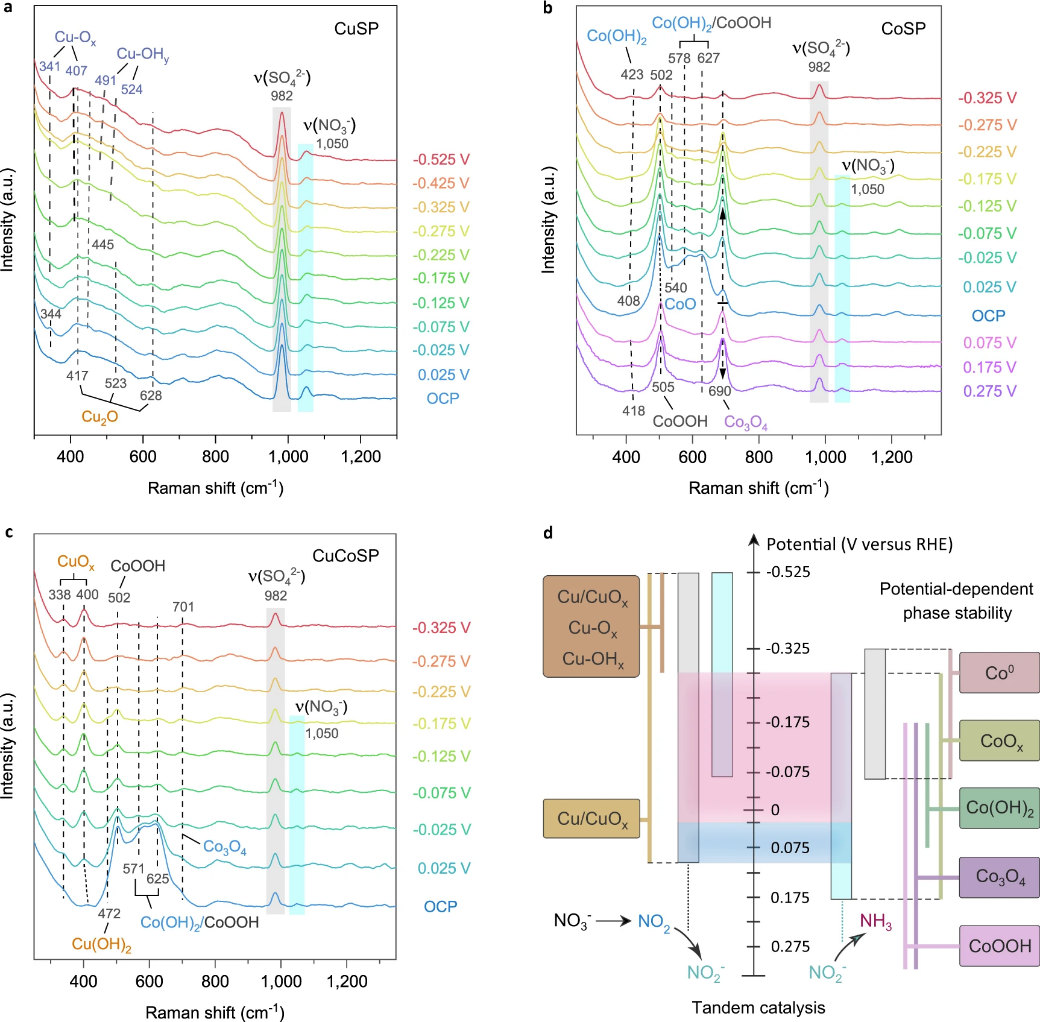
图 5:催化剂的原位拉曼光谱和CuCoSP催化剂的串联机理示意图。在含有 0.01 M NO3-、0.04 M K2SO4和 0.01 M KOH 的电解质中,CuSP (a)、CoSP (b) 和 CuCoSP (c) 在不同施加电位下的原位拉曼光谱。d 所提出的低过电位下,CuCoSP 串联催化 NO3RR 的反应机理。
04 结论与展望
在这项工作中,作者提出了一种高效的串联催化剂的概念,该概念涉及过渡金属与电位相关的中间相的耦合,以作为级联 NO3- 到 NH3转化的协同催化位点。此外,作者使用具有明确空间排列的 Cu/CuOx–Co/CoO 杂化物验证了这一概念,具体而言,通过 Cu/Co基二元金属硫化物的电化学氧化还原活化诱导相重构来实现了这一概念。在该串联催化系统中,NO3- 离子优先在 Cu/CuOx相上还原为 NO2-,而 NO2-中间体随后被转移并选择性地在 Co/CoO 相上转化为 NH3。 在两个不同的相邻金属/金属氧化物相上,依次还原 NO3- 和 NO2-能够在低过电位下高速生成 NH3。在 -0.175 V vs RHE 时,所设计的 CuCoSP 催化剂在 pH 13 的 0.1 M NO3- 溶液中表现出高的 NH3FE(90.6%)和高达 1.17 mmol cm-2 h-1的YNH3,优于大多数相同条件下的 NO3RR催化剂。尽管串联催化广泛用于非均相系统,但本研究直接证明了使用不同的中间相作为串联催化位点的可能性。这种拼接过渡金属活性相的概念可设计用于多步化学反应的高性能、多功能电催化剂,例如通过将 NO3RR 与 CO2 还原相结合进行尿素电合成。




暂无评论
发表评论